题目内容
下列有关化学用语表示正确的是( )
A、N2的电子式: |
| B、氯化钠的分子式:NaCl |
C、S2-的结构示意图: |
| D、乙烯的结构简式:C2H4 |
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.氮气分子中,氮原子最外层达到8电子稳定结构,漏掉了氮原子的一对未成键电子;
B.氯化钠为离子化合物的,不存在氯化钠分子;
C.硫离子的核电荷数为16,核外电子总数为18,最外层为8个电子;
D.乙烯分子中含有官能团碳碳双键,结构简式中没有标出碳碳双键.
B.氯化钠为离子化合物的,不存在氯化钠分子;
C.硫离子的核电荷数为16,核外电子总数为18,最外层为8个电子;
D.乙烯分子中含有官能团碳碳双键,结构简式中没有标出碳碳双键.
解答:
解:A.氮气分子中存在氮氮三键,氮原子最外层达到8电子稳定结构,氮气正确的电子式为: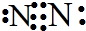 ,故A错误;
,故A错误;
B.NaCl为氯化钠的化学式,氯化钠晶体为离子晶体,不存在氯化钠分子,故B错误;
C.硫离子核电荷数为16,最外层达到8电子稳定结构,硫离子结构示意图为: ,故C正确;
,故C正确;
D.乙烯分子中含有碳碳双键,结构简式中必须标出其官能团,乙烯正确的结构简式为:CH2=CH2,故D错误;
故选C.
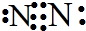 ,故A错误;
,故A错误;B.NaCl为氯化钠的化学式,氯化钠晶体为离子晶体,不存在氯化钠分子,故B错误;
C.硫离子核电荷数为16,最外层达到8电子稳定结构,硫离子结构示意图为:
 ,故C正确;
,故C正确;D.乙烯分子中含有碳碳双键,结构简式中必须标出其官能团,乙烯正确的结构简式为:CH2=CH2,故D错误;
故选C.
点评:本题考查了电子式、离子结构示意图、化学式与分子式、结构简式等化学用语的判断,题目难度中等,注意掌握常见化学用语的概念及正确的表示方法,明确化学式与分子式、结构简式与结构简式的关系.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列实验方法正确的是( )
| A、欲制备Fe(OH)3胶体,向盛有沸水的烧杯中滴加FeCl3饱和溶液并长时间煮沸 |
| B、加入适量NaOH溶液后过滤,以除去KCl溶液中少量的MgCl2 |
| C、测定溶液pH,用玻璃棒蘸取原溶液点在润湿的pH试纸上立即与比色卡比较 |
| D、滴定时眼睛应注视锥形瓶内溶液的颜色变化而不应注视滴定管内的液面变化 |
下列有关叙述正确的是( )
| A、氢键是一种特殊化学键,它广泛地存在于自然界中 |
B、在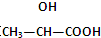 分子中含有1个手性C原子 分子中含有1个手性C原子 |
| C、碘单质在水溶液中溶解度很小是因为I2和H2O都是非极性分子 |
| D、含氧酸可用通式XOm(OH)n来表示,若n值越大,则含氧酸的酸性越大 |
酒后驾车是引发交通事故的重要原因.交警对驾驶员进行呼气酒精检测的原理是:橙色的K2Cr2O7酸性水溶液遇乙醇迅速生成蓝绿色的Cr3+.下列对乙醇的描述与此测定原理有关的是( )
①乙醇密度比水小 ②乙醇沸点低 ③乙醇有还原性④乙醇是烃的含氧衍生物.
①乙醇密度比水小 ②乙醇沸点低 ③乙醇有还原性④乙醇是烃的含氧衍生物.
| A、②④ | B、②③ | C、①④ | D、①③ |
手性分子是指在分子结构 中,当a、b、c、d为彼此互不相同的原子或原子团时,称此分子为手性分子,中心碳原子为手性碳原子.下列分子中指定的碳原子(用★标记)属于手性碳原子的是( )
中,当a、b、c、d为彼此互不相同的原子或原子团时,称此分子为手性分子,中心碳原子为手性碳原子.下列分子中指定的碳原子(用★标记)属于手性碳原子的是( )
 中,当a、b、c、d为彼此互不相同的原子或原子团时,称此分子为手性分子,中心碳原子为手性碳原子.下列分子中指定的碳原子(用★标记)属于手性碳原子的是( )
中,当a、b、c、d为彼此互不相同的原子或原子团时,称此分子为手性分子,中心碳原子为手性碳原子.下列分子中指定的碳原子(用★标记)属于手性碳原子的是( )A、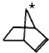 降冰片烯 |
B、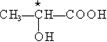 乳酸 |
C、 苯甲醇 |
D、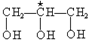 甘油 |
已知水和苯互不相溶,苯不与钠反应,在烧杯中加水和苯(密度:0.88g/cm3)各50mL.将一小粒金属钠(密度:0.97g/cm3)投入烧杯中,观察到的现象可能是( )
| A、钠在水层中反应并四处游动 |
| B、钠停留在苯层中不发生反应 |
| C、钠在苯的液面上反应并四处游动 |
| D、钠在苯与水的界面处反应并可能做上、下跳动 |
常温下,PH=3的HCl和PH=11的NH3?H2O等体积混合反应后,溶液中各离子浓度大小比较是( )
| A、C(Cl-)>C(NH4+)>C(H+)>C(OH-) |
| B、C(NH4+)>C(Cl-)>C(H+)>C(OH-) |
| C、C(NH4+)>C(Cl-)>C(OH-)>C(H+) |
| D、C(Cl-)>C(NH4+)>C(OH-)>C(H+) |
化学与社会、生产、生活紧切相关,下列说法正确的是( )
| A、为了治理酸雨污染,政府应取缔硫酸厂、火电厂、水泥厂等 |
| B、我国是稀土储量大国,可以大量开采稀土矿卖给全世界,赚取外汇 |
| C、减少燃煤的使用,改用风能、太阳能等能源,符合“低碳生活”理念 |
| D、由铝土矿(主要含Al2O3,还含有Fe2O3、SiO2等杂质)冶炼金属铝的过程中,只涉及复分解反应 |
 ⅢA族的硼、铝、镓、铟、铊等元素和ⅤA族的氮、磷、砷、锑、铋等元素形成的化合物在研究和生产中有许多重要用途.请回答下列问题.
ⅢA族的硼、铝、镓、铟、铊等元素和ⅤA族的氮、磷、砷、锑、铋等元素形成的化合物在研究和生产中有许多重要用途.请回答下列问题.