题目内容
某学习小组研究铁和硝酸银溶液的反应,并检验铁的氧化产物.
实验操作和现象:
(1)根据上述实验现象,铁和硝酸银溶液的反应的离子方程式为 .
(2)甲同学认为,实验IV说明溶液中不含Fe3+.乙同学不同意,设计并完成了实验V:
取1mL Fe(NO3)3溶液,滴加2滴等浓度的KSCN溶液,振荡,溶液变红;再加入少量AgNO3溶液,溶液红色褪去,产生白色沉淀.
①乙同学实验的结论是 ;
②用平衡移动原理解释,实验V中溶液红色褪去的原因是 .
(3)丙同学向实验IV所得的溶液中,继续滴加KSCN溶液,边滴边振荡,观察到白色沉淀逐渐增多,最终溶液变红.丙同学由此认为,铁和硝酸银溶液的反应还有Fe3+生成.你是否同意他的观点,理由是 .
(4)丁同学向丙同学实验所得的红色体系中,继续滴加浓KSCN溶液,边滴边振荡,发现溶液红色逐渐加深,最后,白色沉淀逐渐溶解,得到深血红色溶液.
资料表明,硫氰化银白色沉淀能溶于含有SCN-的溶液中,生成无色的Ag(SCN)43-AgSCN+3SCN-?Ag(SCN)43-.
①实验中,溶液红色逐渐加深的可能原因是 ;
②为便于观察研究,丁同学希望稀释最终所得的深血红色溶液,得到浅红色溶液.你预计,加水稀释时的现象是:溶液红色变浅、 .
实验操作和现象:
| 实验序号 | 实验操作 | 实验现象 |
| Ⅰ | 将一束光亮洁净的铁丝伸入AgNO3溶液中,一段时间后,过滤. | 铁丝表面有银白色固体析出,溶液逐渐变为浅绿色 |
| Ⅱ | 取少量滤液,滴加几滴稀盐酸 | 有白色沉淀生成 |
| Ⅲ | 另取少量滤液,滴入K3[Fe(CN)6]溶液 | 有蓝色沉淀生成 |
| IV | 另取少量滤液,滴入KSCN溶液,振荡 | 溶液不变红,出现白色沉淀 |
(2)甲同学认为,实验IV说明溶液中不含Fe3+.乙同学不同意,设计并完成了实验V:
取1mL Fe(NO3)3溶液,滴加2滴等浓度的KSCN溶液,振荡,溶液变红;再加入少量AgNO3溶液,溶液红色褪去,产生白色沉淀.
①乙同学实验的结论是
②用平衡移动原理解释,实验V中溶液红色褪去的原因是
(3)丙同学向实验IV所得的溶液中,继续滴加KSCN溶液,边滴边振荡,观察到白色沉淀逐渐增多,最终溶液变红.丙同学由此认为,铁和硝酸银溶液的反应还有Fe3+生成.你是否同意他的观点,理由是
(4)丁同学向丙同学实验所得的红色体系中,继续滴加浓KSCN溶液,边滴边振荡,发现溶液红色逐渐加深,最后,白色沉淀逐渐溶解,得到深血红色溶液.
资料表明,硫氰化银白色沉淀能溶于含有SCN-的溶液中,生成无色的Ag(SCN)43-AgSCN+3SCN-?Ag(SCN)43-.
①实验中,溶液红色逐渐加深的可能原因是
②为便于观察研究,丁同学希望稀释最终所得的深血红色溶液,得到浅红色溶液.你预计,加水稀释时的现象是:溶液红色变浅、
考点:性质实验方案的设计,铁及其化合物的性质实验
专题:实验设计题
分析:(1)铁丝表面有银白色固体析出,溶液逐渐变为浅绿色,说明铁置换出银,且被氧化生成亚铁离子;
(2)滴加KSCN和AgNO3溶液生成白色沉淀,沉淀为AgSCN,结合平衡移动解答该题;
(3)在滴加、振荡过程中,空气中氧气氧化亚铁离子生成铁离子;
(4)继续滴加浓KSCN溶液,SCN-浓度增大,且空气氧化亚铁离子生成铁离子,铁离子浓度也增大,有利于平衡正向移动;
加水稀释,溶液浓度降低,颜色变浅,SCN-浓度降低,且生成AgSCN白色沉淀.
(2)滴加KSCN和AgNO3溶液生成白色沉淀,沉淀为AgSCN,结合平衡移动解答该题;
(3)在滴加、振荡过程中,空气中氧气氧化亚铁离子生成铁离子;
(4)继续滴加浓KSCN溶液,SCN-浓度增大,且空气氧化亚铁离子生成铁离子,铁离子浓度也增大,有利于平衡正向移动;
加水稀释,溶液浓度降低,颜色变浅,SCN-浓度降低,且生成AgSCN白色沉淀.
解答:
解:(1)铁丝表面有银白色固体析出,溶液逐渐变为浅绿色,说明铁置换出银,且被氧化生成亚铁离子,反应的离子方程式为Fe+2Ag+=Fe2++2Ag,
故答案为:Fe+2Ag+=Fe2++2Ag;
(2)①再加入少量AgNO3溶液,溶液红色褪去,产生白色沉淀,可说明Ag+的存在干扰用KSCN对Fe3+的检验,故答案为:Ag+的存在干扰用KSCN对Fe3+的检验;
②滴加KSCN和AgNO3溶液生成白色沉淀,沉淀为AgSCN,导致SCN-浓度降低,使平衡Fe3++3SCN-?Fe(SCN)3逆向移动,溶液红色褪去,
故答案为:加入AgNO3溶液后,Ag++SCN-=AgSCN↓,使SCN-浓度降低,促使平衡Fe3++3SCN-?Fe(SCN)3逆向移动,溶液红色褪去;
(3)不能同意丙同学的看法,在滴加、振荡过程中,空气中氧气氧化亚铁离子生成铁离子,故答案为:不同意,实验过程中空气中的氧气将亚铁离子氧化生成铁离子;
(4)①继续滴加浓KSCN溶液,SCN-浓度增大,且空气氧化亚铁离子生成铁离子,铁离子浓度也增大,有利于平衡正向移动,
故答案为:加KSCN溶液,SCN-浓度增大,同时空气氧化亚铁离子生成铁离子,铁离子浓度也增大,都促使Fe3++3SCN-?Fe(SCN)3正向移动,溶液红色逐渐加深;
②加水稀释,溶液浓度降低,颜色变浅,已知硫氰化银白色沉淀能溶于含有SCN-的溶液中,则SCN-浓度降低,可生成AgSCN白色沉淀,故答案为:白色沉淀.
故答案为:Fe+2Ag+=Fe2++2Ag;
(2)①再加入少量AgNO3溶液,溶液红色褪去,产生白色沉淀,可说明Ag+的存在干扰用KSCN对Fe3+的检验,故答案为:Ag+的存在干扰用KSCN对Fe3+的检验;
②滴加KSCN和AgNO3溶液生成白色沉淀,沉淀为AgSCN,导致SCN-浓度降低,使平衡Fe3++3SCN-?Fe(SCN)3逆向移动,溶液红色褪去,
故答案为:加入AgNO3溶液后,Ag++SCN-=AgSCN↓,使SCN-浓度降低,促使平衡Fe3++3SCN-?Fe(SCN)3逆向移动,溶液红色褪去;
(3)不能同意丙同学的看法,在滴加、振荡过程中,空气中氧气氧化亚铁离子生成铁离子,故答案为:不同意,实验过程中空气中的氧气将亚铁离子氧化生成铁离子;
(4)①继续滴加浓KSCN溶液,SCN-浓度增大,且空气氧化亚铁离子生成铁离子,铁离子浓度也增大,有利于平衡正向移动,
故答案为:加KSCN溶液,SCN-浓度增大,同时空气氧化亚铁离子生成铁离子,铁离子浓度也增大,都促使Fe3++3SCN-?Fe(SCN)3正向移动,溶液红色逐渐加深;
②加水稀释,溶液浓度降低,颜色变浅,已知硫氰化银白色沉淀能溶于含有SCN-的溶液中,则SCN-浓度降低,可生成AgSCN白色沉淀,故答案为:白色沉淀.
点评:本题综合考查物质的性质实验,为高考常见题型,侧重于学生的分析能力和实验能力的考查,注意把握题给信息以及实验的原理、方法,为解答该题的关键,答题时注意审题,难度较大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列化学反应对应的离子方程式正确的是( )
| A、KOH溶液与KHSO4溶液反应:OH-+H+═H2O |
| B、稀H2SO4与Ba(OH)2溶液反应:H++SO42-+OH-+Ba2+═BaSO4↓+H2O |
| C、铁与盐酸反应:Fe+2H+═Fe3++H2↑ |
| D、AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
具备基本的化学实验技能是进行科学探究的基础和保证.下列有关实验操作正确的是:( )
A、 点燃酒精灯 |
B、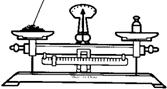 称量固体 |
C、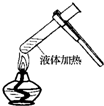 液体加热 |
D、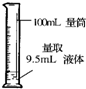 量取液体 |
下列各组比较项目包含的数据关系中,前者比后者大的是( )
A、
| ||
| B、CH3COOH分别跟H-18O-C2H5和H-16O-C2H5发生酯化反应后,生成酯的相对分子质量 | ||
| C、乙炔(C2H2)与苯(C6H6)中的碳碳键键长 | ||
| D、等质量的甲醇与乙二醇,与足量金属Na反应生成的氢气 |
