题目内容
2.下列哪位科学家根据a粒子散射实验提出了原子结构的有核模型( )| A. | 道尔顿 | B. | 卢瑟福 | C. | 汤姆生 | D. | 玻尔 |
分析 根据原子结构模型的演变可知:
(1)19世纪初,英国科学家道尔顿提出近代原子学说,他认为原子是微小的不可分割的实心球体;
(2)1897年,英国科学家汤姆生发现了电子.1904年提出“葡萄干面包式”的原子结构模型;
(3)1911年英国物理学家卢瑟福(汤姆生的学生)提出了带核的原子结构模型;
(4)1913年丹麦物理学家波尔(卢瑟福的学生)引入量子论观点,提出电子在一定轨道上运动的原子结构模型;
(5)奥地利物理学家薛定谔提出电子云模型(几率说).
解答 解:A.道尔顿提出了近代原子学说,故A错误;
B.卢瑟福(汤姆生的学生)提出了带核的原子结构模型,故B正确;
C.汤姆生发现了电子,提出“葡萄干面包式”的原子结构模型,故C错误;
D.波尔提出了量子论,故D错误.
故选B.
点评 本题主要考查了化学史,难度不大,平时注意知识的积累.

练习册系列答案
相关题目
12.为了加快漂白粉的作用,最好的方法是( )
| A. | 加入苛性钠溶液 | B. | 用水湿润 | C. | 加少量盐酸 | D. | 加干燥剂使用 |
13.肼(N2H4)是火箭发动机的一种燃料,反应时N2O4为氧化剂,生成N2和H2O(g),已知:
N2(g)+2O2(g)═N2O4(g),△H=+8.7kJ/mol;
N2H4(g)+O2(g)═N2(g)+2H2O(g),△H=-534.0kJ/mol;
下列表示肼跟N2O4反应的热化学反应方程式,正确的是( )
N2(g)+2O2(g)═N2O4(g),△H=+8.7kJ/mol;
N2H4(g)+O2(g)═N2(g)+2H2O(g),△H=-534.0kJ/mol;
下列表示肼跟N2O4反应的热化学反应方程式,正确的是( )
| A. | 2N2H4(g)+N2O4(g)═3N2(g)+4H2O(g);△H=-542.7 kJ/mol | |
| B. | 2N2H4(g)+N2O4(g)═3N2(g)+4H2O(g);△H=-1059.3 kJ/mol | |
| C. | N2H4(g)+$\frac{1}{2}$N2O4(g)═$\frac{3}{2}$N2(g)+2H2O(g);△H=-1076.7 kJ/mol | |
| D. | 2N2H4(g)+N2O4(g)═3N2(g)+4H2O(g);△H=-1076.7 kJ/mol |
10.下列分子中所有原子都满足最外层为8电子结构的是( )
| A. | NH3 | B. | PCl3 | C. | PCl5 | D. | BCl3 |
17.历史上最早应用的还原性染料是靛蓝,其结构简式如图所示,下列关于靛蓝的叙述中错误的是( )
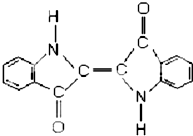

| A. | 靛蓝由碳、氢、氧、氮四种元素组成 | B. | 它的分子式是 C16H10N2O2 | ||
| C. | 该物质是苯的同系物 | D. | 它含有碳碳双键、羰基等官能团 |
14.燃烧1g乙醇(液态)生成CO2气体和液态水放出热量为29.7KJ,则乙醇燃烧的热化学方程式正确的是( )
| A. | C2H5OH+3O2═2CO2+3H2O△H=-29.7 kJ/mol | |
| B. | C2H5OH(l)+3O2 (g)═2CO2 (g)+3H 2 O(l)△H=-1366.2kJ/mol | |
| C. | C2 H5 OH(l)+3O2 (g)═2CO2 (g)+3H 2O(g)△H=+29.7 kJ/mol | |
| D. | C2H5OH(l)+3O2 (g)═2CO2 (g)+3H 2 O(l)△H=+1366.2kJ/mol |
11.在一定温度下,密闭容器中可逆反应N2(g)+3H2(g)?2NH3(g)达到平衡的标志是( )
| A. | 混合气体的密度不再发生变化 | |
| B. | 单位时间内生成nmolN2的同时生成3nmolH2 | |
| C. | N2、H2、NH3的浓度不再发生变化 | |
| D. | N2、H2、NH3的物质的量之比为1:3:2 |
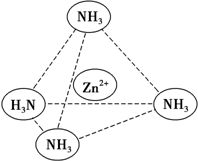 锌是一种重要的金属,锌及其化合物有着广泛的应用.
锌是一种重要的金属,锌及其化合物有着广泛的应用.