题目内容
下列物质的熔、沸点高低顺序正确的是( )
| A、金刚石>晶体硅>二氧化硅 |
| B、HI>HBr>HCl>HF |
| C、NaF>NaCl>NaBr |
| D、NaCl>Hg>S |
考点:晶体的类型与物质熔点、硬度、导电性等的关系
专题:化学键与晶体结构
分析:A.原子晶体中半径越小,键长越短,共价键越强,熔点越大;
B.氢化物中分子间存在氢键的熔沸点较高;
C.离子晶体中离子半径越小,电荷越大,熔点越大;
D.离子晶体的熔沸点一般高于分子晶体,Hg常温下为液体.
B.氢化物中分子间存在氢键的熔沸点较高;
C.离子晶体中离子半径越小,电荷越大,熔点越大;
D.离子晶体的熔沸点一般高于分子晶体,Hg常温下为液体.
解答:
解:A.原子晶体中半径越小,键长越短,共价键越强,熔点越大,因键长C-C<O-Si<Si-Si,则熔沸点为金刚石>二氧化硅>晶体硅,故A错误;
B.氢化物中分子间存在氢键的熔沸点较高,没有氢键时,相对分子质量越大,分子间作用力越强,熔沸点越高,则熔沸点为HF>HI>HBr>HCl,故B错误;
C.因离子半径F-<Cl-<Br-,则熔点为NaF>NaCl>NaBr,故C正确;
D.离子晶体的熔沸点一般高于分子晶体,Hg常温下为液体,所以熔沸点:NaCl>S>Hg,故D错误;
故选C.
B.氢化物中分子间存在氢键的熔沸点较高,没有氢键时,相对分子质量越大,分子间作用力越强,熔沸点越高,则熔沸点为HF>HI>HBr>HCl,故B错误;
C.因离子半径F-<Cl-<Br-,则熔点为NaF>NaCl>NaBr,故C正确;
D.离子晶体的熔沸点一般高于分子晶体,Hg常温下为液体,所以熔沸点:NaCl>S>Hg,故D错误;
故选C.
点评:本题考查晶体熔点的比较,明确不同类型晶体熔点的比较方法是解答本题的关键,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
一定温度下,向饱和Na2SO4溶液中加入ag无水Na2SO4粉末,搅拌、静置后析出bgNa2SO4?10H2O晶体,则bg-ag的值是( )
| A、原饱和溶液中减少的Na2SO4的质量 |
| B、原饱和溶液中失去的水的质量 |
| C、原饱和溶液中失去的水和NaSO4的质量总和 |
| D、析出晶体中含有的Na2SO4的质量 |
A、B属于短周期中不同主族的元素,A、B原子的最外层电子中,成对电子和未成对电子占据的轨道数相等,若A元素的原子序数为a,则B元素的原子序数为( )
| A、a-4 | B、a+1 |
| C、a+3 | D、a+4 |
下列说法错误的是( )
| A、医学上用于消毒的酒精是75%酒精溶液 |
| B、单质硅是将太阳能转化为电能的常用材料 |
| C、食醋是含3%~5%乙酸的溶液 |
| D、乙醇可做为提取碘水中碘的萃取剂 |
有关甲醛(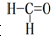 )、苯、二氧化碳及水说法不正确的是( )
)、苯、二氧化碳及水说法不正确的是( )
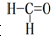 )、苯、二氧化碳及水说法不正确的是( )
)、苯、二氧化碳及水说法不正确的是( )| A、苯与B3N3H6互为等电子体,且分子中原子共平面 |
| B、甲醛、苯和二氧化碳中碳原子均采用sp2杂化 |
| C、苯、二氧化碳是非极性分子,水和甲醛是极性分子 |
| D、水的沸点比甲醛高得多,是因为水分子间能形成氢键,而甲醛分子间不能形成氢键 |
下列所述变化规律正确的是( )
| A、Na、Mg、Al还原性依次增强 |
| B、HCl、PH3、H2S稳定性依次减弱 |
| C、LiOH、NaOH、KOH碱性依次减弱 |
| D、O2-、F-、Na+、Mg2+的离子半径依次减小 |
 一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是( )
一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是( )| A、该反应的化学方程式为3B+4D?6A+2C |
| B、反应进行到1s时,v(A)=v(D) |
| C、反应进行到6s时,各物质的百分含量不变 |
| D、反应进行到6s时,B的平均反应速率为0.05mol/(L?min) |
构成SiO2的化学键在性质上和构成CO2分子的共价键都是极性键,所以( )
| A、SiO2和CO2都属于原子晶体 |
| B、SiO2和CO2都是分子晶体 |
| C、前者是原子晶体,后者是分子晶体 |
| D、前者是分子晶体,后者是原子晶体 |