题目内容
某种SO2与CO2组成的混合气体,其密度是同条件下氧气密度的1.5倍,由此可知该混合气体中SO2的质量分数为( )
| A、20% | B、80% |
| C、73.3% | D、26.7% |
考点:物质的量的相关计算
专题:计算题
分析:根据混合气体相等氧气的密度计算混合气体平均相对分子质量,令SO2与CO2的物质的量分别为xmol、ymol,根据平均相对分子质量确定二者物质的量之比,进而计算SO2的质量分数.
解答:
解:SO2与CO2组成的混合气体的平均相对分子质量为1.5×32=48,
令SO2与CO2的物质的量分别为xmol、ymol,则:
=48
整理得x:y=1:4,
该混合气体中SO2的质量分数为
×100%=26.7%,
故选D.
令SO2与CO2的物质的量分别为xmol、ymol,则:
| 64x+44y |
| x+y |
整理得x:y=1:4,
该混合气体中SO2的质量分数为
| 1mol×64g/mol |
| 1mol×64g/mol+4mol×44g/mol |
故选D.
点评:本题考查混合物计算,难度不大,关键是计算各组分的各物质的物质的量之比.

练习册系列答案
相关题目
下列关于臭氧的叙述中正确的是( )
| A、臭氧与氧气是氧元素的两种同素异形体,其物理性质相同 |
| B、打雷时、高压电机和复印机工作时均会产生臭氧 |
| C、臭氧能与Ag、Hg等与氧气不易反应的物质发生化学反应 |
| D、臭氧的密度大于空气,故臭氧主要集中在地面 |
下列各组离子能在溶液中大量共存的是( )
| A、H+、ClO-、S2-、Na+ | ||||
B、H+、I-、N
| ||||
| C、K+、Cl-、ClO-、Na+ | ||||
D、Cu2+、Cl-、N
|
下列实验操作与实验目的不一致的是( )
| A、向试管中加入相同体积浓度为0.005 mol?L-1的FeCl3溶液和0.01 mol?L-1的KSCN溶液,再加入几滴饱和FeCl3溶液; 证明增大反应物浓度,平衡向正反应方向移动. |
| B、将Cl2通入0.1 mol?L-1KBr溶液中,再加入少量CCl4,振荡; 证明氯、溴的非金属性强弱. |
| C、用饱和Na2CO3溶液可将BaSO4转化为BaCO3; 证明Ksp(BaCO3)>Ksp(BaSO4). |
| D、用pH计测定0.1 mol?L-1醋酸溶液的Ph; 证明醋酸在水溶液中部分电离. |
(双选)下列说法中正确的是( )
| A、如果某一反应的反应物能量总和高于生成物能量总和,则该反应是吸热反应 |
| B、我国目前使用最多的燃料是酒精 |
| C、煤炭直接燃烧不仅产生大量烟尘,而且生成SO2,导致酸雨的形成 |
| D、煤经过处理后制得水煤气、干馏煤气等,可提高燃烧效率和减少环境污染 |
下列说法正确的是( )
| A、铁溶于稀硝酸,溶液变黄:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O |
| B、向氢氧化亚铁中加入足量的稀硝酸:Fe(OH)2+2H+═Fe2++2H2O |
| C、向含有少量FeCl3的MgCl2溶液中加入足量Mg(OH)2粉末,搅拌一段时间后过滤,目的是除去MgCl2溶液中少量的FeCl3 |
| D、用FeCl3溶液腐蚀铜线路板:Cu+Fe3+═Cu2++Fe2+ |
根据有机物 的结构推测,它不可能发生的反应是( )
的结构推测,它不可能发生的反应是( )
 的结构推测,它不可能发生的反应是( )
的结构推测,它不可能发生的反应是( )| A、银镜反应 | B、加成反应 |
| C、酯化反应 | D、中和反应 |
醇类化合物在香料中占有重要的地位,下面所列的是一些天然的或合成的醇类香料:
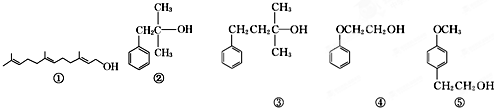
下列说法中正确的是( )

下列说法中正确的是( )
| A、可用酸性KMnO4溶液检验①中是否含有碳碳双键 |
| B、②和③互为同系物,均能催化氧化生成醛 |
| C、④和⑤互为同系物,可用核磁共振氢谱检验 |
| D、等物质的量的上述5种有机物与足量的金属钠反应,消耗钠的量相同 |
我国具有悠久的酿酒历史,某白酒标签上标有“53°”字样,它表示( )
| A、该酒是在53℃条件下酿制的 |
| B、该酒的着火点为53℃ |
| C、100 mL该酒中含有53 mL酒精 |
| D、100g该酒中含有53g酒精 |