题目内容
13.把18.0mol/L的浓硫酸稀释成2.00mol/L的稀硫酸100mL.(1)实验操作如下,正确的操作步骤是③④⑥⑤⑧⑦②①(填序号).
①将配好的稀硫酸倒入试剂瓶中,贴好标签
②盖好容量瓶塞,反复颠倒,摇匀
③用量筒量取11.1mL的18.0mol/L的浓硫酸
④将浓硫酸沿烧杯内壁慢慢注入盛有少量水的烧杯中
⑤用少量蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液也全部转移到容量瓶中
⑥将已冷却至室温的硫酸溶液沿玻璃棒注入100mL的容量瓶中
⑦改用胶头滴管滴加蒸馏水,使溶液凹面恰好与刻度线相切
⑧继续向容量瓶中加蒸馏水,直到液面接近刻度线1至2cm处
(2)下列操作对所配溶液浓度造成的后果,请选填“偏高”、“偏低”或“无影响”.
①未洗涤稀释过浓硫酸的小烧杯偏低;
②使用经蒸馏水洗涤后未干燥的小烧杯稀释浓硫酸无影响;
③加水时不慎超过了刻度线,又将超出部分用吸管吸出偏低;
④配溶液用的容量瓶用蒸馏水洗涤后未经干燥无影响;
⑤定容时俯视刻度偏高;
⑥倒转容量瓶摇匀后,液面降至刻度线下,再加水至刻度偏低.
⑦用NaOH配制溶液时称量时间过长偏低.
分析 (1)依据配制一定物质的量浓度溶液的一般步骤排序解答;
(2)分析操作对溶质的物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行误差分析;
解答 解;(1)用浓溶液配制一定物质的量浓度稀溶液的一般配制步骤是计算、量取、稀释、冷却、移液、洗涤、定容、摇匀、装瓶可知正确的操作顺序为:③④⑥⑤⑧⑦②①,故答案为:③④⑥⑤⑧⑦②①;
(2)①未洗涤稀释过浓硫酸的小烧杯偏低;
②使用经蒸馏水洗涤后未干燥的小烧杯稀释浓硫酸,对溶质的物质的量和溶液体积都不会产生影响,溶液浓度无影响;
故答案为:无影响;
③加水时不慎超过了刻度线,又将超出部分用吸管吸出,导致溶质部分损耗,溶质的物质的量偏大,溶液浓度偏低;
故答案为:偏低;
④配溶液用的容量瓶用蒸馏水洗涤后未经干燥,对溶质的物质的量和溶液体积都不会产生影响,溶液浓度无影响;
故答案为:无影响;
⑤定容时俯视刻度导致溶液体积偏小,溶液浓度偏高;
故答案为:偏高;
⑥倒转容量瓶摇匀后,液面降至刻度线下,再加水至刻度导致溶液体积偏大,溶液浓度偏低;
故答案为:偏低;
⑦用NaOH配制溶液时称量时间过长,导致溶质中含有氢氧化钠的物质的量偏小,溶液浓度偏低;
故答案为:偏低.
点评 本题考查了一定物质的量浓度溶液的配制过程中的计算和误差分析,明确配制原理及步骤是解题关键,注意误差分析的方法和技巧.

练习册系列答案
相关题目
8.只用一种试剂鉴别NH4Cl、KCl、Na2SO3、和(NH4)2SO4,该试剂是( )
| A. | BaCl2溶液 | B. | NaOH溶液 | C. | Ba(OH)2溶液 | D. | AgNO3溶液 |
9.将2mol A气体和1mol B气体在固定体积的密闭容器中混合并在一定条件下发生如下反应并达到平衡状态:2A(g)+B(g)?2C(g),此反应为放热反应.下列能增大正、逆反应速率的方法是:
(1)再充入1mol A气体;(2)充入2mol的惰性气体;(3)加入正催化剂;(4)升高温度;(5)移走部分C气体.
其中正确的是( )
(1)再充入1mol A气体;(2)充入2mol的惰性气体;(3)加入正催化剂;(4)升高温度;(5)移走部分C气体.
其中正确的是( )
| A. | (1)(3)(5) | B. | (1)(3)(4) | C. | (1)(2)(4)(5) | D. | (1)(2)(3)(4)(5) |
1.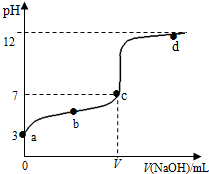 在常温下向20mL 0.1mol•L-1 某酸(用HA表示)溶液中逐滴加入0.1mol•L-1 NaOH溶液,用pH计来测定溶液中pH数据如下表,作出pH与NaOH溶液体积关系的曲线如图所示(忽略温度变化).请根据表中数据和滴定曲线回答以下问题:
在常温下向20mL 0.1mol•L-1 某酸(用HA表示)溶液中逐滴加入0.1mol•L-1 NaOH溶液,用pH计来测定溶液中pH数据如下表,作出pH与NaOH溶液体积关系的曲线如图所示(忽略温度变化).请根据表中数据和滴定曲线回答以下问题:
(1)实验中的指示剂最好使用酚酞;
(2)当V (NaOH)=20.00mL时,请写出溶液中主要存在的两种平衡体系是A-+H2O?HA+OH-、H2O?H++OH-;
溶液中离子浓度由大到小的顺序是c(Na+)>c(A-)>c(OH-)>c(H+);
(3)a、b、c、d四点对应溶液中水的电离程度由大到小的顺序是c>b>a>d.
(4)该温度下,滴定曲线上c点时HA的电离平衡常数Ka=$\frac{1{0}^{-7}V}{20-V}$.(用含V的代数简式表示)
 在常温下向20mL 0.1mol•L-1 某酸(用HA表示)溶液中逐滴加入0.1mol•L-1 NaOH溶液,用pH计来测定溶液中pH数据如下表,作出pH与NaOH溶液体积关系的曲线如图所示(忽略温度变化).请根据表中数据和滴定曲线回答以下问题:
在常温下向20mL 0.1mol•L-1 某酸(用HA表示)溶液中逐滴加入0.1mol•L-1 NaOH溶液,用pH计来测定溶液中pH数据如下表,作出pH与NaOH溶液体积关系的曲线如图所示(忽略温度变化).请根据表中数据和滴定曲线回答以下问题:| V(NaOH)mL | 0.00 | 10.00 | 18.00 | 19.80 | 19.98 | 20.00 | 20.02 | 20.20 | 22.00 | 40.00 |
| pH | 3.0 | 4.7 | 5.7 | 6.7 | 7.7 | 8.7 | 9.7 | 10.7 | 11.7 | 12.5 |
(2)当V (NaOH)=20.00mL时,请写出溶液中主要存在的两种平衡体系是A-+H2O?HA+OH-、H2O?H++OH-;
溶液中离子浓度由大到小的顺序是c(Na+)>c(A-)>c(OH-)>c(H+);
(3)a、b、c、d四点对应溶液中水的电离程度由大到小的顺序是c>b>a>d.
(4)该温度下,滴定曲线上c点时HA的电离平衡常数Ka=$\frac{1{0}^{-7}V}{20-V}$.(用含V的代数简式表示)
8.下列对于NH3和CO2的说法中正确的是( )
| A. | 都是直线形结构 | |
| B. | 中心原子都采取sp1杂化 | |
| C. | NH3为三角锥形结构,CO2为直线形结构 | |
| D. | 氮原子和碳原子上都没有孤对电子 |
18.如表为某食品包装袋上的说明书:
(1)选择说明书中的物质回答下面的问题:
①能水解生成氨基酸的物质是蛋白质.
②若人体缺少维生素A,易患夜盲症.
(2)对芝麻酱说明书的判断正确的是C (填序号).
A.不含微量元素 B.不含糖类和油脂
C.婴儿最不宜食用 D.钙含量低于豆腐和鸡蛋.
| 芝麻酱每100 g含有 蛋白质:19.2 g 脂肪:52.7 g 碳水化合物16.8 g 维生素 A:17 μg 铁:50.3 mg 硒:4 μg 含钙:相当于300 g豆腐 含铁:相当于800 g鸡蛋 (提醒:芝麻酱可引起部分婴儿过敏性皮炎) |
①能水解生成氨基酸的物质是蛋白质.
②若人体缺少维生素A,易患夜盲症.
(2)对芝麻酱说明书的判断正确的是C (填序号).
A.不含微量元素 B.不含糖类和油脂
C.婴儿最不宜食用 D.钙含量低于豆腐和鸡蛋.
5.下列两种物质不属于同分异构体的是( )
| A. | 葡萄糖和果糖 | B. | 蔗糖和麦芽糖 | C. | 淀粉和纤维素 | D. | 正丁烷和异丁烷 |
3.下列物质间有如下反应关系,已知A是某两种溶质的混合溶液,判断下列选项正确的是( )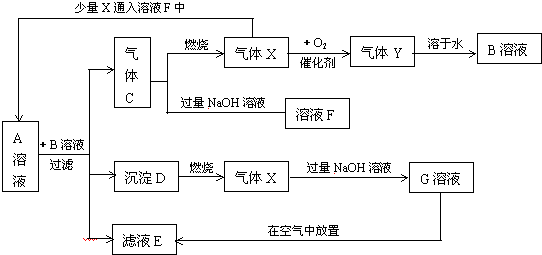

| A. | 气体C是SO2 | |
| B. | 溶液A和溶液B可能的化学反应为3Na2S+Na2SO3+4H2SO4=3S↓+H2S↑+4Na2SO4+3H2O | |
| C. | 若氧气足量气体C可以一步反应得到气体Y | |
| D. | 图中少量X通入溶液F中不涉及氧化还原反应 |
 .
.