题目内容
写电离方程式:(1)H2SO4 ; (2)NaHCO3 、 .
考点:电离方程式的书写
专题:电离平衡与溶液的pH专题
分析:(1)硫酸为强酸,在溶液中完全电离出氢离子和硫酸根离子,电离方程式用等号;
(2)碳酸氢钠为强电解质,在溶液中电离出钠离子和碳酸氢根离子,另外碳酸氢根离子能够电离出氢离子和碳酸根离子.
(2)碳酸氢钠为强电解质,在溶液中电离出钠离子和碳酸氢根离子,另外碳酸氢根离子能够电离出氢离子和碳酸根离子.
解答:
解:(1)硫酸是强电解质,溶液中能完全电离出氢离子和硫酸根离子,电离方程式为:H2SO4=2H++SO42-,
故答案为:H2SO4=2H++SO42-;
(2)碳酸氢钠在水中电离出钠离子和碳酸氢根离子,电离方程式为NaHCO3═Na++HCO3-;碳酸氢根离子能够电离出碳酸根离子和氢离子,其电离方程式为:HCO3-?H++CO32-,
故答案为:NaHCO3═Na++HCO3-;HCO3-?H++CO32-.
故答案为:H2SO4=2H++SO42-;
(2)碳酸氢钠在水中电离出钠离子和碳酸氢根离子,电离方程式为NaHCO3═Na++HCO3-;碳酸氢根离子能够电离出碳酸根离子和氢离子,其电离方程式为:HCO3-?H++CO32-,
故答案为:NaHCO3═Na++HCO3-;HCO3-?H++CO32-.
点评:本题考查了电离方程式的书写,侧重基础知识的考查,题目难度不大,注意掌握强弱电解质的概念,明确电离方程式的书写方法,试题有利于培养学生灵活应用所学知识的能力.

练习册系列答案
相关题目
分析下列各物质的物理性质,可判断其固态不属于分子晶体的是( )
| A、碳化铝,黄色晶体,熔点2200℃.熔融态不导电 |
| B、溴化铝,无色晶体,熔点98℃,熔融态不导电 |
| C、五氟化钒,无色晶体,熔点19.5℃,易溶于乙醇、氯仿、丙铜中 |
| D、干冰,无色晶体,熔融时不导电 |
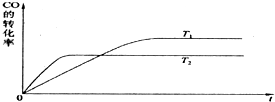 实际上电离平衡、盐的水解平衡等,它们都可看作是化学平衡的一种.请根据所学化学知识回答下列问题:
实际上电离平衡、盐的水解平衡等,它们都可看作是化学平衡的一种.请根据所学化学知识回答下列问题: