题目内容
12.下列离子方程式书写正确的是( )| A. | Na投入到水中:Na+H2O═Na++OH-+H2↑ | |
| B. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| C. | Al2O3和NaOH溶液:Al2O3+2OH-═2AlO2-+H2O | |
| D. | FeCl2溶液跟Cl2反应:Fe2++Cl2═Fe3++2Cl- |
分析 A.原子个数不守恒;
B.一水合氨为弱碱,应保留化学式;
C.二者反应生成偏铝酸钠和水;
D.电荷不守恒.
解答 解:A.Na投入到水中,离子方程式:2Na+2H2O═2Na++2OH-+H2↑,故A错误;
B.在氯化铝溶液中加入过量氨水,离子方程式应为:Al3++3NH3•H2O=Al(OH)3↓+3 NH4+,故B错误;
C.Al2O3和NaOH溶液,离子方程式:Al2O3+2OH-═2AlO2-+H2O,故C正确;
D.FeCl2溶液跟Cl2反应,离子方程式:F2e2++Cl2═2Fe3++2Cl-,故D错误;
故选:C.
点评 本题考查离子方程式的书写,明确反应实质及离子方程式书写方法是解题关键,注意离子反应应遵循原子个数、电荷数守恒规律,注意化学式的拆分,题目难度不大.

练习册系列答案
相关题目
2.钯的化合物氯化钯可用来检测有毒气体CO,常温发生反应的化学方程式为:CO+PdCl2+H2O═CO2+Pd↓+2HC1,下列说法正确的是( )
| A. | 氧化性:PdCl2>CO2 | |
| B. | 生成22.4LCO2时,转移的电子为2mo1 | |
| C. | 反应中PdCl2被氧化 | |
| D. | CO气体只有在高温下才能表现还原性 |
4.下列反应都在恒温、恒压下进行,在较高温度和较低温度下都能自发进行的是( )
| A. | Ag+(aq)+Cl-(aq)═AgCl(s)△H=-51.1 kJ•mol-1 | |
| B. | 2K(s)+2H2O(l)═2K+(aq)+2OH-(aq)+H2(g)△H=-393.2 kJ•mol-1 | |
| C. | 2Mg(s)+O2(g)═2MgO(s)△H=-1203.2 kJ•mol-1 | |
| D. | CaCO3(s)═CaO(s)+CO2(g)△H=+178.2 kJ•mol-1 |
1.下列化学用语表示正确的是( )
| A. | 原子核中有7个中子的碳原子:12C | |
| B. | 明矾的电离方程式是:KAl(SO4)2•12H2O═K++Al3++2SO42-+12H2O | |
| C. | K+结构示意图: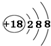 | |
| D. | Ba(OH)2与H2SO4反应的化学方程式是:Ba(OH)2+H2SO4═BaSO4↓+H2O |
2.下列叙述不正确的是( )
| A. | 强电解质溶液的导电能力不一定比弱电解质溶液的导电能力强 | |
| B. | 影响化学平衡常数的因素是温度 | |
| C. | 放热反应不一定能自发进行,而吸热反应也可能自发进行 | |
| D. | 熵增大的反应其焓变一定增大,焓变增大的反应其熵不一定增大 |

 工艺流程如图.
工艺流程如图.