题目内容
已知:C(s)+
O2(g)=CO(g)△H=-akJ/mol
CO(g)+
O2(g)=CO2(g)△H=-bkJ/mol
求:2C(s)+2O2(g)=2CO2(g)△H= .
| 1 |
| 2 |
CO(g)+
| 1 |
| 2 |
求:2C(s)+2O2(g)=2CO2(g)△H=
考点:用盖斯定律进行有关反应热的计算
专题:
分析:已知:①C(s)+
O2(g)=CO(g)△H=-akJ/mol
②CO(g)+
O2(g)=CO2(g)△H=-bkJ/mol
由盖斯定律可知,(①+②)×2得2C(s)+2O2(g)=2CO2(g)△H.
| 1 |
| 2 |
②CO(g)+
| 1 |
| 2 |
由盖斯定律可知,(①+②)×2得2C(s)+2O2(g)=2CO2(g)△H.
解答:
解:已知:①C(s)+
O2(g)=CO(g)△H=-akJ/mol
②CO(g)+
O2(g)=CO2(g)△H=-bkJ/mol
由盖斯定律可知,(①+②)×2得2C(s)+2O2(g)=2CO2(g)△H=2×[-akJ/mol+(-bkJ/mol)]=-2(a+b)kJ/mol,
故答案为:-2(a+b)kJ/mol.
| 1 |
| 2 |
②CO(g)+
| 1 |
| 2 |
由盖斯定律可知,(①+②)×2得2C(s)+2O2(g)=2CO2(g)△H=2×[-akJ/mol+(-bkJ/mol)]=-2(a+b)kJ/mol,
故答案为:-2(a+b)kJ/mol.
点评:本题考查了盖斯定律的应用,为高考高频考点,难度不大,由已知热化学方程式构造目标热化学方程式是关键,侧重于观察分析能力、计算能力的培养.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
用惰性电极进行电解,下列说法正确的是( )
| A、电解稀硫酸溶液,实质上是电解水,故溶液pH不变 |
| B、电解氯化铜溶液,在阴极上和阳极上析出产物的物质的量之比为1:1 |
| C、电解氯化钠溶液,在阴极上析出钠. |
| D、电解硫酸钠溶液,在阴极上析出O2,在阳极上析出H2 |
下列说法正确的是( )
| A、葡萄糖与淀粉互为同分异构体 |
| B、糖类、油脂、蛋白质都是高分子化合物 |
| C、糖类、油脂、蛋白质都能发生水解 |
| D、油脂有油和脂肪之分,但都属于酯 |
对下列事实的解释错误的是( )
| A、在蔗糖中加入浓硫酸后出现黑色物质,说明浓硫酸具有脱水性 |
| B、浓硝酸在光照下颜色变黄,说明浓硝酸不稳定 |
| C、常温下,浓硝酸可以用铝罐贮存,说明铝与浓硝酸不反应 |
| D、干燥的氯气通入干燥的红色纸条中不褪色,说明氯气本身没有漂白性 |
在水溶液中能大量共存的一组离子是( )
A、SO
| ||||
B、H+、Ca2+、NO
| ||||
C、NH
| ||||
D、K+、Fe3+、SCN-、NO
|
有机物A的结构简式为 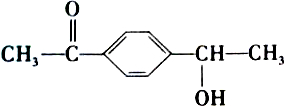 ,有关它的说法正确的是( )
,有关它的说法正确的是( )
 ,有关它的说法正确的是( )
,有关它的说法正确的是( )| A、A遇FeCl3溶液显紫色 |
| B、A被酸性KMnO4溶液氧化可生成羧酸 |
| C、乙酸与A形成的酯的化学式是C12H14O3 |
| D、A能发生取代、加成、消去、氧化、聚合等反应 |
下列说法中正确的是( )
| A、元素性质的周期性变化是指原子半径、元素的主要化合价及原子核外电子排布的周期性变化 |
| B、元素性质的周期性变化决定于元素原子结构的周期性变化 |
| C、从Li→F,Na→Cl,元素的最高化合价均呈现从+1价→+7价的变化 |
| D、电子层数相同的原子核外电子排布,其最外层电子数均从1个到8个呈现周期性变化 |