题目内容
16.如图是部分短周期元素原子半径与原子序数的关系图.字母代表元素,分析正确的是( )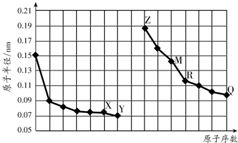
| A. | R在周期表的第15列 | |
| B. | 简单离子的半径:X>Z>M | |
| C. | Y、Q两种元素的气态氢化物及其最高价氧化物的水化物均为强酸 | |
| D. | Z的单质能从M与Q元素构成的盐溶液中置换出单质M |
分析 图中元素分别为第二周期和第三周期元素的原子半径的变化,根据原子序数关系可知X为O元素,Y为F元素,Z为Na元素,M为Al元素,R为Si元素,Q为Cl元素,以此解答该题.
解答 解:图中元素分别为第二周期和第三周期元素的原子半径的变化,根据原子序数关系可知X为O元素,Y为F元素,Z为Na元素,M为Al元素,R为Si元素,Q为Cl元素,
A.R为Si元素,位于周期表第14列,故A错误;
B.O2-、Na+、Al3+离子电子层结构相同,核电荷数越大离子半径越小,故离子半径O2->Na+>Al3+,故B正确;
C.F元素没有最高价含氧酸,故C错误;
D.Na与氯化铝溶液反应,首先与水反应生成氢氧化钠与氢气,氢氧化钠再与氯化铝反应,不能置换出Al,故D错误,
故选B.
点评 本题考查原子结构与元素的性质,为高频考点,侧重于学生的分析能力的考查,元素的推断是解答的关键,注意把握元素的性质及单质、化合物的性质即可解答,题目难度中等.

练习册系列答案
相关题目
3.甲烷分子是以C原子为中心的正四面体结构,而不是正方形的平面结构,理由是( )
| A. | CH3Cl只代表一种物质 | B. | CH2Cl2只代表一种物质 | ||
| C. | CHCl3只代表一种物质 | D. | CCl4是非极性分子 |
7.分子式为C8H8O2的含有苯环有机物,能与NaHCO3溶液反应生成气体,则符合上述条件的同分异构体(不考虑立体异构)有( )
| A. | 4种 | B. | 8种 | C. | 11种 | D. | 12种 |
4.自来水加工处理流程如图,下列有关说法不正确的是( ) 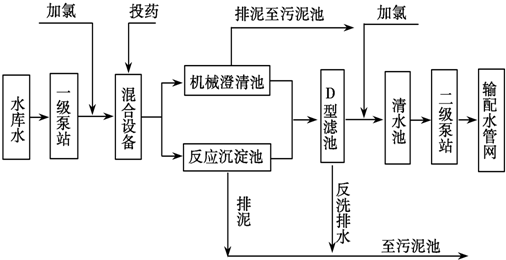

| A. | 若用FeSO4作混凝剂,最终铁将以Fe(OH)2形式进入反应沉淀池 | |
| B. | 投药时常加入适量的石灰,是为了除去水中Mg2+、HCO3-等 | |
| C. | 自来水生产中,前面加氯起消毒杀菌作用,后面加氯是保持水中有效氯的含量,防止自来水二次污染 | |
| D. | 用ClO2消毒自来水,消毒效率是等质量氯气的2.63倍 |
11.为测定人体血液中Ca2+的含量,设计了如下方案:

有关反应的化学方程式为:2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O若血液样品为15mL,滴定生成的草酸消耗0.001mol•L-1的KMnO4溶液15.0mL,则这种血液样品中的含钙量为( )

有关反应的化学方程式为:2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O若血液样品为15mL,滴定生成的草酸消耗0.001mol•L-1的KMnO4溶液15.0mL,则这种血液样品中的含钙量为( )
| A. | 0.002 5 mol•L-1 | B. | 0.001 mol•L-1 | C. | 0.000 3 mol•L-1 | D. | 0.003 5 mol•L-1 |
8.下列有关“化学与生活”的叙述不正确的是( )
| A. | “地沟油”禁止食用,但可以用来制肥皂 | |
| B. | 中国古代利用明矾溶液的酸性清除铜镜表面的铜锈 | |
| C. | 纤维素在人体内可水解为葡萄糖,故可作人类的营养物质 | |
| D. | 葡萄中的花青素在碱性环境下显蓝色,故可用苏打粉检验假红酒 |
6.W、X、Y、Z均为短周期主族元素,原子序数依次增加,且原子核外L电子层的电子数分别为0、5、8、8,它们的最外层电子数之和为10.下列说法正确的是( )
| A. | Z与X的最高价氧化物对应水化物反应可产生W的单质气体 | |
| B. | X、Y、Z三种元素的最高价氧化物对应水化物两两可发生反应 | |
| C. | Y的氧化物都可做呼吸面具的供氧剂 | |
| D. | W与X之间只能形成极性共价化合物 |
 ”和画“×”分别标明B和N的相对位置.
”和画“×”分别标明B和N的相对位置.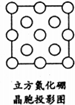

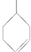 .
.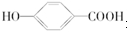 在一定条件下发生聚合反应生成高分子化合物,写出该反应的化学方程式(有机物写结构简式)
在一定条件下发生聚合反应生成高分子化合物,写出该反应的化学方程式(有机物写结构简式) .
.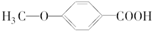 的同分异构体很多,其中符合下列条件的有3种.
的同分异构体很多,其中符合下列条件的有3种. .
.