题目内容
3.将H2S气体通入FeCl3溶液中,得到淡黄色的沉淀.该反应的离子方程式为( )| A. | 2FeCl3+S2-═2FeCl2+S↓ | B. | 2FeCl3+H2S═2FeCl2+S↓+2H++2Cl- | ||
| C. | 2Fe3++S2-═2Fe2++S↓ | D. | 2Fe3++H2S═2Fe2++S↓+2H+ |
分析 三价铁离子具有强的氧化性能够氧化硫化氢生成单质硫,本身被还原为二价铁离子,据此解答.
解答 解:A.电荷不守恒,故A错误;
B.氯化铁为强电解质,应拆成离子形式,故B错误;
C.硫化氢为弱电解质,应保留化学式,故C错误;
D.将H2S气体通入FeCl3溶液中,得到淡黄色的沉淀,离子方程式:2Fe3++H2S═2Fe2++S↓+2H+,故D正确;
故选:D.
点评 本题考查了离子方程式的书写,明确反应实质及离子方程式书写方法是解题关键,注意离子反应必须遵循客观事实,注意离子反应遵循原子个数、电荷数守恒规律,注意化学式的拆分,题目难度不大.

练习册系列答案
相关题目
13.关于图中各装置的叙述不正确的是( )
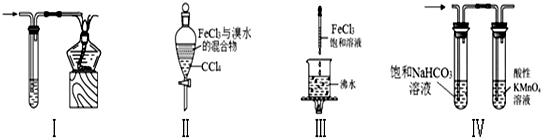

| A. | 装置Ⅰ:可用于处理CO尾气 | |
| B. | 装置Ⅱ:充分振荡后静置,下层溶液为红棕色,上层无色 | |
| C. | 装置Ⅲ:当液体呈红褐色,停止加热,让光束通过体系可产生丁达尔效应 | |
| D. | 装置Ⅳ:可用于除去CO2气体中的HCl和SO2气体 |
11.常温下,下列各组离子在指定的条件下一定能大量共存的是( )
| A. | c(Fe3+)=0.1mol•L-1的溶液中:K+、ClO-、SO42-、SCN- | |
| B. | 在pH=2的溶液中:NH4+、K+、ClO-、Cl- | |
| C. | 在c(H+)/c(OH-)=10-12的溶液中:K+、Na+、C1O-、NO3- | |
| D. | 水电离c(H+)=10-12的溶液中:Mg2+、Cu2+、SO42+、K+ |
18.下列过程属于熵增的是( )
| A. | 水蒸气凝结为液态的水 | B. | 氨气和氯化氢反应生成氯化铵晶体 | ||
| C. | 碳酸氢铵在常温情况下分解 | D. | CO点燃时生成CO2 |
 .
. .
.
