题目内容
下列物质长期暴露在空气中会氧化变质的是( )
| A、CuSO4溶液 |
| B、NaOH溶液 |
| C、FeSO4溶液 |
| D、NaCl溶液 |
考点:铁的氧化物和氢氧化物,钠的重要化合物
专题:元素及其化合物
分析:物质长期暴露在空气中会氧化变质,说明该物质具有强强还原性,容易被空气中的氧气氧化,依据物质的性质判断解答.
解答:
解:A.硫酸铜不具有还原性,在空气中不能被氧化,故A错误;
B.氢氧化钠溶液与空气中的二氧化碳反应而变质,但是不属于氧化反应,故B错误;
C.硫酸亚铁中的二价铁离子具有强的还原性,能被空气中的氧气氧化生成三价铁而变质,故C正确;
D.氯化钠溶液能够稳定存在与空气中不变质,故D错误;
故选:C.
B.氢氧化钠溶液与空气中的二氧化碳反应而变质,但是不属于氧化反应,故B错误;
C.硫酸亚铁中的二价铁离子具有强的还原性,能被空气中的氧气氧化生成三价铁而变质,故C正确;
D.氯化钠溶液能够稳定存在与空气中不变质,故D错误;
故选:C.
点评:本题考查了物质的性质,题目难度不大,明确硫酸亚铁的强的还原性是解题关键,注意审题应仔细.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下[已知N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol]:下列说法正确的是( )
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol N2、3mol H2 | 2mol NH3 | 4mol NH3 |
| NH3的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
| 体系压强(Pa) | p1 | p2 | p3 |
| 反应物转化率 | α1 | α2 | α3 |
| A、2c1>c3 |
| B、a+b>92.4 |
| C、2p2<p3 |
| D、α1+α3<1 |
下列各组混合物的分离或提纯方法正确的是( )
| A、提纯NaCl和KNO3的混合物中的KNO3:加热蒸发、冷却结晶,过滤 |
| B、除去CO2中混有的少量CO:混合气体依次通过NaOH溶液和浓硫酸 |
| C、除去盐酸溶液中混有的少量CaCl2:加入过量CaCO3粉末,过滤 |
| D、将自来水制成蒸馏水:蒸馏 |
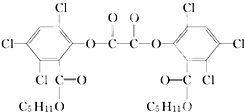 夏日的夜晚,常看见儿童手持发光的“魔棒”在广场上嬉戏.“魔棒”发光原理是利用过氧化氢氧化草酸二酯产生能量,该能量被传递给荧光物质后便发出荧光,草酸二酯(CPPO)结构简式如图.下列有关说法不正确的是( )
夏日的夜晚,常看见儿童手持发光的“魔棒”在广场上嬉戏.“魔棒”发光原理是利用过氧化氢氧化草酸二酯产生能量,该能量被传递给荧光物质后便发出荧光,草酸二酯(CPPO)结构简式如图.下列有关说法不正确的是( )| A、草酸二酯的分子式为C26H24Cl6O8 |
| B、1 mol草酸二酯与氢氧化钠稀溶液反应(苯环上卤素不水解),最多消耗4 mol NaOH |
| C、该有机物能发生加成反应、取代反应、氧化反应 |
| D、1 mol草酸二酯与氢气完全反应,需要氢气6 mol |
常温下,把pH=3的盐酸溶液和pH=10的Ba(OH)2溶液混合,若混合溶液的pH为7,则盐酸溶液和Ba(OH)2溶液的体积比是( )
| A、1:10 | B、1:5 |
| C、1:2 | D、2:1 |
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.高铁电池的总反应为:3Zn+2K2O4+8H2O
3Zn(OH)2+2Fe(OH)3+2Fe(OH)3+4KOH下列叙述不正确的是( )
| 放电 |
| 充电 |
| A、放电时负极反应为:3Zn-6e-+6OH-═3Zn(OH)2 |
| B、放电时正极反应为:2FeO42-+6e-+8H2O═2Fe(OH)3+10OH- |
| C、放电时每转移3mol电子,正极有1mol K2FeO4被氧化 |
| D、放电时正极附近溶液的碱性增强 |