题目内容
4.在恒温容积为2L的密闭容器中进行反应N2(g)+3H2(g)?2NH3(g),若氨气的物质的量由0.4mol降到0.24mol需2s,那么由0.24mol降到0.04mol,需要的反应时间为( )| A. | 等于2.5s | B. | 等于2.0s | C. | 大于2.5s | D. | 小于2.0s |
分析 结合v=$\frac{△c}{△t}$及浓度减小、速率减小来解答.
解答 解:若氨气的物质的量由0.4mol降到0.24mol需2s,那么由0.24mol降到0.04mol,若按照前2s的反应速率计算所需时间,$\frac{\frac{0.4mol-0.24mol}{2L}}{2s}$=$\frac{\frac{0.24mol-0.04mol}{2L}}{t}$,
t=2.5s,但2s后氨气的浓度减小,反应速率减小,则需要时间大于2.5s,
故选C.
点评 本题考查反应速率的计算,为高频考点,把握浓度与速率的关系为解答的关键,侧重分析与计算能力的考查,注意开始反应速率快,题目难度不大.

练习册系列答案
 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
14.下列关于有机物的说法中正确的是( )
| A. | 卤代烷水解时,从氟到碘,由于非金属性依次减弱,所以水解越来越困难 | |
| B. | 溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+═AgBr↓ | |
| C. | 相同碳原子数的多卤代烃,随着卤原子数的增多,密度依次降低 | |
| D. | 常温下,CH3Cl是气体,甲烷的其他3种氯代产物都是液体 |
15.下列关于实验的说法错误的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 检验CO2与NaOH溶液反应后 的溶液中是否有Na2CO3 | 取少量反应后的溶液,滴加BaC12溶液,看是否有沉淀生成 |
| B | 除去甲烷中含有的乙烯杂质 | 将气体通入到酸性高锰酸钾溶液后,再通过装有碱石灰的干燥管 |
| C | 证明酸性:H2CO3>H3BO3 | 向Na2CO3中滴入过量H3BO3溶液,无气泡冒出 |
| D | 分离Fe(OH)3胶体和FeCl3溶液 | 将混合液倒入过滤器中过滤 |
| A. | A | B. | B | C. | C | D. | D |
12.下列说法不正确的是( )
| A. | 麦芽糖及其水解产物均能发生银镜反应 | |
| B. | 用溴水即可鉴别苯酚溶液、2,4-己二烯和甲苯 | |
| C. | 在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH | |
| D. | 用甘氨酸( 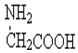 )和丙氨酸( )和丙氨酸( 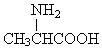 )缩合最多可形成4种二肽(不考虑形成环状) )缩合最多可形成4种二肽(不考虑形成环状) |
19.已知2SO2(g)+O2(g)?2SO3(g)为放热反应,对该反应的下列说法正确的是( )
| A. | 1mol O2的能量一定高于2mol SO2的能量 | |
| B. | 1mol SO2的能量一定高于1mol SO3的能量 | |
| C. | 因为该反应是放热反应,所以不必加热就可以发生 | |
| D. | 2mol SO3的能量一定低于2mol SO2和1mol O2的总能量 |
9.现有三组混合液:
①乙酸乙酯和乙酸钠溶液;
②乙醇和丁醇;
③NaBr和单质Br2的水溶液.
分离以上各混合液的正确方法依次是( )
①乙酸乙酯和乙酸钠溶液;
②乙醇和丁醇;
③NaBr和单质Br2的水溶液.
分离以上各混合液的正确方法依次是( )
| A. | 分液、蒸馏、萃取 | B. | 萃取、蒸馏、分液 | C. | 分液、萃取、蒸馏 | D. | 蒸馏、萃取、分液 |
16.日本福岛核泄露事故的铯-137其符号表示为${\;}_{55}^{137}$Cs,下列关于该原子的说法不正确的是( )
| A. | 质子数为137 | B. | 质子数为55 | ||
| C. | 电子数为82 | D. | 中子数与质子数之差为27 |
13.下列属于电解质的是( )
| A. | 铜 | B. | 氨水 | C. | 氧化钠 | D. | 蔗糖 |
14.下列操作的原理或对应的离子方程式不正确的是( )
| A. | Mg (HCO3)2溶液中加入足量的Ba(OH)2:Mg2++2HCO3-+2Ba2++4OH-═Mg(OH)2↓+2BaCO3↓+2H2O | |
| B. | Na2S2O3溶液中加入稀硫酸:S2O32-+2H+═SO2↑+S↓+H2O | |
| C. | K2Cr2O7溶液中加入氢氧化钠溶液,溶液颜色由橙色变成黄色,证明溶液中存在平衡:Cr2O72-+H2O?2CrO42-+2H+ | |
| D. | 用浓盐酸酸化的KMnO4溶液与H2O2混合来证明H2O2具有还原性:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O |