题目内容
设NA为阿伏加德罗常数的数值,下列叙述正确的是(相对原子量:H—1 C—12)
| A.1 mol/L氯化铜溶液中的Cu2+数小于NA |
| B.标准状况下,22.4 L Cl2参加任何化学反应转移的电子数都是2NA |
| C.28 g聚乙烯含有的碳原子数为2NA |
| D.1 mol CH5+所含电子数为8NA |
C
解析试题分析:A.却体积无法计算。错误。B.标准状况下,22.4 L Cl2参加任何化学反应转移的电子数可能是2NA如Na2S+Cl2 =2NaCl+ S↓;也可能是1mol.如:Cl2+H2O HCl+HClO。错误。C.聚乙烯的链节为—CH2CH2—,式量为28,酸雨28 g聚乙烯含有的碳原子数为2NA。正确。D.在1个CH5+所含电子数为10个,所以1 mol CH5+所含电子数为8NA.错误。
HCl+HClO。错误。C.聚乙烯的链节为—CH2CH2—,式量为28,酸雨28 g聚乙烯含有的碳原子数为2NA。正确。D.在1个CH5+所含电子数为10个,所以1 mol CH5+所含电子数为8NA.错误。
考点:考查阿伏加德罗常数的有关计算的知识。

练习册系列答案
相关题目
NA表示阿伏加德罗常数的数值,下列说法正确的是
| A.用石墨电极电解Ca(NO3)2溶液,当转移电子数为0.2 NA时,阴极析出4 g金属 |
| B.0.1 mol24Mg32S晶体中所含中子总数为2.8 NA |
| C.常温下含有NA个NO2、N2O4分子的混合气体,温度降至标准状况,其体积约为22.4 L |
| D.在熔融状态下,1 mol NaHSO4完全电离出的阳离子数目为2 NA |
化学科学需要借助化学专用语言描述,下列有关化学用语正确的是( )
A.H2O的电子式: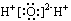 |
B.质量数为14的碳原子: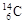 |
C.CO2的比例模型: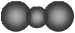 |
D.Cl-的结构示意图: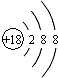 |
下列叙述能肯定金属A 比金属B更活泼的是
| A.A原子的最外层电子数比B原子的最外层电子数少 |
| B.A原子的电子层数比B原子多 |
| C.1 mol A从酸中置换出H2比1 mol B多 |
| D.常温下,A能从酸中置换出氢气,而B不能 |
日本福岛第一核电站泄漏出微量的钚(Pu)-239。下列关于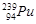 叙述准确的是
叙述准确的是
| A.原子序数是239 | B.质量数是94 | C.中子数是239 | D.质子数是94 |
在1L/mol氨水中,下列叙述正确的是( )
| A.含1molNH3·H2O |
| B.含NH3、NH4+之和为1mol |
| C.只含有1molNH3 |
| D.NH3、NH3·H2O、NH4+之和为1mol |
下列化学用语正确的是( )
A.聚丙烯的结构简式: |
B.四氯化碳分子的电子式: |
C.2-乙基-1,3-丁二烯分子的键线式: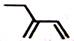 |
D.丙烷分子的比例模型: |
下列说法正确的是
| A.1L 1mol?L-1的NH4Cl溶液中一定含有NA个NH4+ |
| B.常温常压下,22.4L乙烯中含共价键数为5 NA |
| C.6.8g熔融的KHSO4中含有0.05 NA个阳离子 |
| D.1mol冰醋酸和lmo1乙醇在浓硫酸加热下反应可生成NA个H2O |
某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+、Al3+和K+,取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉淀;过滤,洗涤,灼烧,得到1.6g固体;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀.由此可知原溶液中
| A.至少存在5种离子 |
| B.Cl-一定存在,且c(Cl?)≥0.4mol/L |
| C.SO42-、NH4+、一定存在,Cl-可能不存在 |
| D.CO32-、Al3+一定不存在,K+可能存在 |