题目内容
 乙酸是食醋的主要成分,它具有以下化学性质:
乙酸是食醋的主要成分,它具有以下化学性质:(1)可使紫色石蕊试液变
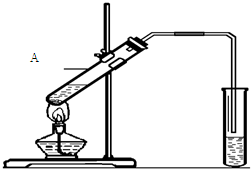
(2)能发生酯化反应.实验室用如图所示装置制取乙酸乙酯,请写出该反应的化学方程式:
考点:乙酸乙酯的制取
专题:实验题
分析:(1)乙酸含官能团羧基,乙酸为弱酸,具有酸的通性;
(2)乙醇和乙酸在浓硫酸催化作用下生成乙酸乙酯,据此分析.
(2)乙醇和乙酸在浓硫酸催化作用下生成乙酸乙酯,据此分析.
解答:
解:(1)乙酸含官能团羧基,乙酸为弱酸,具有酸的通性,可使紫色石蕊变红,
故答案为:红;酸;
(2)乙醇和乙酸在浓硫酸催化作用下生成乙酸乙酯,反应方程式为:CH3COOH+C2H5OH
CH3COOC2H5+H2O,
故答案为:CH3COOH+C2H5OH
CH3COOC2H5+H2O.
故答案为:红;酸;
(2)乙醇和乙酸在浓硫酸催化作用下生成乙酸乙酯,反应方程式为:CH3COOH+C2H5OH
| 浓硫酸 |
| △ |
故答案为:CH3COOH+C2H5OH
| 浓硫酸 |
| △ |
点评:本题考查了乙酸的性质,较基础,注意乙酸的官能团为羧基,乙酸的性质酸性和酯化反应都是羧基所体现的.

练习册系列答案
相关题目
有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下由此可判断这四种金属的活动性顺序是( )
| 实验 装置 |  |  |  |  |
| 部分实 验现象 | a极质量减小,b极质量增大 | b极有气体产生,c极无变化 | d极溶解,c极有气体产生 | 电流从a极流向d极 |
| A、a>b>c>d |
| B、b>c>d>a |
| C、d>a>b>c |
| D、a>b>d>c |
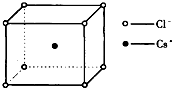 如图是氯化铯晶体的晶胞,已知晶体中2个最近的Cl-离子核间距为a cm,氯化铯的摩尔质量为M,NA为阿伏加德罗常数,则氯化铯晶体的密度为( )
如图是氯化铯晶体的晶胞,已知晶体中2个最近的Cl-离子核间距为a cm,氯化铯的摩尔质量为M,NA为阿伏加德罗常数,则氯化铯晶体的密度为( )A、
| ||
B、
| ||
C、
| ||
D、
|
FeCl3+Cu=2FeCl2+CuCl2.该反应利用了铜的什么性质( )
| A、氧化性 | B、还原性 |
| C、导电性 | D、导热性 |
在进行中和热的测定中,下列操作或说法错误的是( )
| A、不可将温度计当搅拌棒使用,也不可靠在容器内壁上 |
| B、搅拌时,环形玻璃搅拌棒应上下移动 |
| C、测量反应混合液的温度时要随时读取温度,记录下最高温度 |
| D、为了使反应完全,必须保证酸和碱恰好完全反应 |
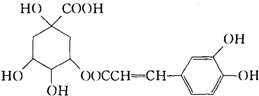 咖啡鞣酸具有较广泛的抗菌作用,其结构简式如图所示:1mol咖啡鞣酸与NaOH完全反应时可消耗 NaOH物质的量是( )
咖啡鞣酸具有较广泛的抗菌作用,其结构简式如图所示:1mol咖啡鞣酸与NaOH完全反应时可消耗 NaOH物质的量是( )| A、2 molNaOH |
| B、4 molNaOH |
| C、6 molNaOH |
| D、8 molNaOH |
金属的腐蚀造成了相当大的经济损失和环境污染,因此,人们想了很多方法防止金属的腐蚀.下面关于金属腐蚀的叙述正确的是( )
| A、铁壳轮船在河水中航行比在海水中航行更易被腐蚀 |
| B、常温下,铁易被干燥的氯气腐蚀 |
| C、钢铁发生吸氧腐蚀时,发生的负极反应为02+4e-+2H20═40H- |
| D、为了防止枪炮表面的钢铁被腐蚀,可以在钢铁表面进行烤蓝处理 |