题目内容
根据反应3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O 回答下列问题:
(1)氧化剂是 ,氧化产物是 。
(2)氧化剂与氧化产物的物质的量比是 。
(3)当有2 mol HNO3被还原时,被氧化的物质的质量为 ,反应中转移的电子数为 ;
(4)有下列6种物质:K2SO4、K2SO3、I2、H2SO4、KIO3、H2O组成一个氧化还原反应,已知在反应中K2SO3失去电子。请回答下列问题:
将这6种物质分别填入下面对应的横线上,组成一个化学方程式(不需配平):
________+________+________ → ________+________+________
(1)HNO3 Cu(NO3)3 (2)2:3 (3)192g 6NA或3.612×1024
(4)K2SO3 + KIO3 + H2SO4 →I2 + K2SO4 + H2O
【解析】
试题分析:在反应中铜的化合价由0→+2价,被氧化,作还原剂生成氧化产物Cu(NO3)3。HNO3中氮的化合价由+5→+2价,被还原,作氧化剂,生成还原产物N0。在反应中8 mol HNO3反应,只有2mol HNO3作氧化剂,其质量为3mol×64g∕mol=192g.氧化剂与氧化产物的物质的量比,2:3.转移转移的电子数为:3×2NA=6NA=3.612×1024。在反应中K2SO3失去电子,说明它是还原剂,被氧化成K2SO4,给定的物质有强氧化性可以作氧化剂的的是KIO3,KIO3在酸性条件下表现氧化性生成的还原产物I2,根据化学反应的过程就是原子重新组合的过程可知:这几种物质组合的反应为K2SO3 + KIO3 + H2SO4 →I2 + K2SO4 + H2O。
考点:考查氧化还原反应等知识。


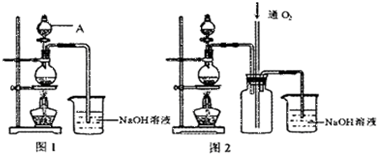
 某同学利用下列装置实现铜与浓硝酸、稀硝酸反应,过程如图所示:
某同学利用下列装置实现铜与浓硝酸、稀硝酸反应,过程如图所示: