题目内容
短周期元素W、X、Y、Z的原子序数依次增大,W与Y,X与Z位于同一主族.W与X可形成共价化合物WX2,分子中各原子均达到8e-稳定结构.Y原子的内层电子总数是其最外层电子数的2.5倍.下列叙述中不正确的是( )
| A、W、X、Y分别为C、O、Si | B、WX2和ZX2的均含极性键 | C、Z的气态氢化物比Y的稳定 | D、原子半径大小顺序为X<W<Y<Z |
分析:Y原子的内层电子总数是其最外层电子数的2.5倍,核外各层电子分别为2、8、4,应为Si元素,W与Y位于同一主族,则W为C元素,W与X可形成共价化合物WX2,分子中各原子均达到8e-稳定结构,说明X应为第ⅥA族元素,结合原子序数小于Y,则应为O元素,X与Z位于同一主族,则Z为S元素,结合对应单质、化合物的性质以及元素周期律知识解答该题.
解答:解:Y原子的内层电子总数是其最外层电子数的2.5倍,核外各层电子分别为2、8、4,应为Si元素,W与Y位于同一主族,则W为C元素,W与X可形成共价化合物WX2,分子中各原子均达到8e-稳定结构,说明X应为第ⅥA族元素,结合原子序数小于Y,则应为O元素,X与Z位于同一主族,则Z为S元素,
A.有以上分析可知W、X、Y分别为C、O、Si,故A正确;
B.CO2和SO2的均含极性键,分别为C=O和S=O键,故B正确;
C.Z为S,Y为Si,S的非金属性比Si强,则Z的气态氢化物比Y的稳定,故C正确;
D.同周期元素的原子半径逐渐减小,则Si>S,故D错误.
故选:D.
A.有以上分析可知W、X、Y分别为C、O、Si,故A正确;
B.CO2和SO2的均含极性键,分别为C=O和S=O键,故B正确;
C.Z为S,Y为Si,S的非金属性比Si强,则Z的气态氢化物比Y的稳定,故C正确;
D.同周期元素的原子半径逐渐减小,则Si>S,故D错误.
故选:D.
点评:本题考查原子结构与元素周期律的关系,为高考常见题型,侧重于学生的分析能力的考查,题目难度不大,本题的关键是根据原子结构特点正确推断元素的种类.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案
相关题目
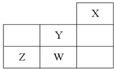 短周期元素W、X、Y、Z在元素周期表中的位置如图所示.下列说法中不正确的是( )
短周期元素W、X、Y、Z在元素周期表中的位置如图所示.下列说法中不正确的是( )| A、X元素形成的单质中存在非极性共价键 | B、W的最高价氧化物对应的水化物是强酸 | C、Y的原子半径在同周期主族元素中最小 | D、Z的气态氢化物的稳定性在同主族元素中最强 |
