题目内容
一定条件下,可逆反应N2 +3H2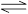 2NH3(正反应为放热反应)达到平衡,当单独改变下述条件后,有关叙述错误的是
2NH3(正反应为放热反应)达到平衡,当单独改变下述条件后,有关叙述错误的是
A、加催化剂,V正、V逆 都发生变化,且变化的倍数相等
B、加压,V正、V逆 都增大,且V正 增大的倍数大于V逆 增大的倍数
C、降温,V正、V逆 都减小,且V正 减小的倍数大于V逆 减小的倍数
D、增大氮气的浓度,V正、V逆 都增大,且V正 增大倍数大于V逆 增大倍数;N2 转换率减小,H2转化率增大
【答案】
C
【解析】催化剂能改变反应的活化能,所以能同等程度改变正逆反应速率,A正确。反应是体积减小的反应,所以增大压强,正反应速率增大的倍数大于逆反应速率增大的倍数,平衡显正反应方向移动,B正确。正反应是放热反应,所以降低温度,正逆反应速率都是降低的,但逆反应速率降低的倍数大正反应速率降低的倍数,平衡向正反应方向移动,C不正确。增大氮气的浓度,平衡向正反应方向移动,氢气转化率增大,氮气转化率降低,D正确,答案选C。

练习册系列答案
相关题目
 B+3C,在下列四种状态中处于平衡的是( )
B+3C,在下列四种状态中处于平衡的是( )