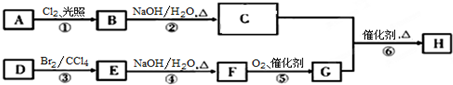
题目内容
关于CH3COONa与CH3COOH的混合溶液,下列关系正确的是
| pH | 离子浓度关系 | |
| A | pH<7 | c(CH3COO-)>c(CH3COOH) |
| B | pH>7 | c(CH3COO-)<c(CH3COOH) |
| C | pH=7 | c(CH3COO-)=c(CH3COOH) |
| D | pH<7 | c(CH3COO-)<c(CH3COOH) |
| A、A | B、B | C、C | D、D |
考点:弱电解质在水溶液中的电离平衡,盐类水解的应用
专题:电离平衡与溶液的pH专题
分析:A.常温下,CH3COONa与CH3COOH的混合溶液中,若混合液的pH<7,以酸的电离为主;
B.若pH>7,则以盐的水解为主,水解程度一般较小;
C.若pH=7,根据电荷守恒分析和水解程度分析;
D.若混合液的pH<7,以酸的电离为主.
B.若pH>7,则以盐的水解为主,水解程度一般较小;
C.若pH=7,根据电荷守恒分析和水解程度分析;
D.若混合液的pH<7,以酸的电离为主.
解答:
解:A.常温下,CH3COONa与CH3COOH的混合溶液的pH<7,以酸的电离为主,弱酸部分电离,则c(CH3COO-)<c(CH3COOH),故A错误;
B.若pH>7,则以盐的水解为主,水解程度一般较小,则:c(CH3COO-)>c(CH3COOH),故B错误;
C.混合液的pH=7,则:c(OH?)=c(H+),根据电荷守恒c(CH3COO?)+c(OH?)=c(H+)+c(Na+)可得:c(CH3COO?)=c(Na+),醋酸的浓度很小,则c(CH3COO-)>c(CH3COOH),故C错误;
D.混合溶液的pH<7,以酸的电离为主,弱酸只有小部分电离,则c(CH3COO-)<c(CH3COOH),故D正确;
故选D.
B.若pH>7,则以盐的水解为主,水解程度一般较小,则:c(CH3COO-)>c(CH3COOH),故B错误;
C.混合液的pH=7,则:c(OH?)=c(H+),根据电荷守恒c(CH3COO?)+c(OH?)=c(H+)+c(Na+)可得:c(CH3COO?)=c(Na+),醋酸的浓度很小,则c(CH3COO-)>c(CH3COOH),故C错误;
D.混合溶液的pH<7,以酸的电离为主,弱酸只有小部分电离,则c(CH3COO-)<c(CH3COOH),故D正确;
故选D.
点评:本题考查混合液中离子浓度大小比较,题目难度中等,试题有利于培养学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
相关题目
下列书写或说法正确的是( )
| A、聚丙烯的链节是-CH2-CH2-CH2- | |||
B、向苯酚溶液中滴加Na2CO3溶液: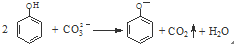 | |||
C、CH3COOH+CH3CH218OH
| |||
| D、苯的同系物能使酸性高锰酸钾溶液褪色,说明烃基对苯环的性质产生了较大的影响 |
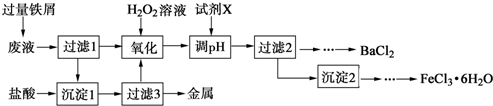
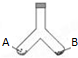 如图所示是一密闭容器,已知A端盛2.3g金属钠,B端盛有xgHgO,当同时加热容器的两侧支管时,钠着火燃烧,冷却后测得容器中空气成分并未发生变化,求x的值.(Hg的相对原子质量是200.6)
如图所示是一密闭容器,已知A端盛2.3g金属钠,B端盛有xgHgO,当同时加热容器的两侧支管时,钠着火燃烧,冷却后测得容器中空气成分并未发生变化,求x的值.(Hg的相对原子质量是200.6)