题目内容
下列标明电子转移的方向和数目的化学方程式中正确的是( )
A、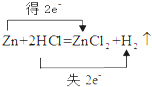 |
B、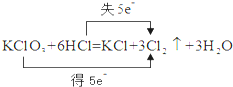 |
C、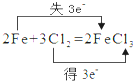 |
D、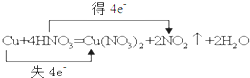 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:A.Zn失去电子,H得到电子;
B.Cl元素的化合价由+5降低为0,得到电子,HCl中Cl失去电子;
C.2molFe失去6mol电子,转移电子数错误;
D.Cu与浓硝酸反应转移的电子数为2.
B.Cl元素的化合价由+5降低为0,得到电子,HCl中Cl失去电子;
C.2molFe失去6mol电子,转移电子数错误;
D.Cu与浓硝酸反应转移的电子数为2.
解答:
解:A.Zn失去电子,H得到电子,则应为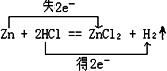 ,故A错误;
,故A错误;
B.Cl元素的化合价由+5降低为0,得到电子,HCl中Cl失去电子,图中方向数目均正确,故B正确;
C.2molFe失去6mol电子,转移电子数错误,应为 ,故C错误;
,故C错误;
D.Cu与浓硝酸反应转移的电子数为2,所以电子转移的方向和数目为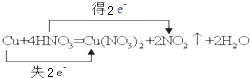 ,故D错误;
,故D错误;
故选B.
 ,故A错误;
,故A错误;B.Cl元素的化合价由+5降低为0,得到电子,HCl中Cl失去电子,图中方向数目均正确,故B正确;
C.2molFe失去6mol电子,转移电子数错误,应为
 ,故C错误;
,故C错误;D.Cu与浓硝酸反应转移的电子数为2,所以电子转移的方向和数目为
 ,故D错误;
,故D错误;故选B.
点评:本题考查氧化还原反应转移电子数,明确得失电子及数目为解答的关键,注意把握双线桥法标电子转移方法、数目的方法,题目难度不大.

练习册系列答案
相关题目
固体NH4I放入一个体积为VL的真空密闭容器中,加热至一定温度后,恒温下发生下列反应:NH4I(s)?NH3(g)+HI(g);2HI(g)?H2(g)+I2(g).平衡时,测得容器中气体共为5mol,其中HI为1.5mol,则下列说法正确的是( )
| A、平衡时氨气为2.5mol | ||
| B、平衡时HI的分解率为20% | ||
| C、若开始时放入固体NH4I的量增大一倍,则平衡时气体共为10 mol | ||
D、其他条件不变把容器的体积缩小到
|
能促进水的电离,并使溶液中c(H+)>c(OH-)的操作是( )
| A、将水加热煮沸 |
| B、向水中投入一小块金属钠 |
| C、向水中通CO2 |
| D、向水中加入明矾晶体 |
当电解质溶液为氢氧化钾水溶液的氢氧燃料电池电解饱和碳酸钠溶液一段时间,假设电解时温度不变且用惰性电极,下列说法正确的是( )
| A、当电池负极消耗m g气体时,电解池阳极同时有m g气体生成 |
| B、电解后c(Na2CO3)不变,且溶液中有晶体析出 |
| C、电池的负极反应式为:O2+2H2O+4e-═4OH- |
| D、电池中c(KOH)不变 |
二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构与双氧水分子相似.常温下,S2Cl2是一种橙黄色液体,遇水易水解,并产生能使品红褪色的气体.下列说法中错误的是( )
| A、S2Cl2的结构式为Cl-S-S-Cl |
| B、S2Cl2为含有极性键和非极性键的极性分子 |
| C、S2Br2与S2Cl2结构相似,熔沸点S2Cl2>S2Br2 |
| D、2S2Cl2+2H2O=SO2↑+3S↓+4HCl |
如图是X、Y两种固体物质的溶解度曲线,下列说法不正确的是( )
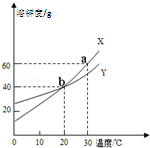

| A、将20℃的饱和溶液X降温到10℃,溶液X仍然是饱和溶液 |
| B、a点表示30℃时,X的溶解度为60g |
| C、b点表示20℃时,X、Y的溶解度相等 |
| D、同质量的X、Y饱和溶液分别从30℃降到10℃时,析出的Y的质量大于X的质量 |
常温下c(H+)最小的是( )
| A、pH=0的溶液. |
| B、0.03 mol?L-1 H2SO4. |
| C、0.05 mol?L-1 HClO |
| D、0.05 mol?L-1的NaHSO4. |
分子是构成物质的一种粒子.走近鲜饼屋,能闻到香味,这是因为( )
| A、分子是不断运动的 |
| B、分子能保持物质的化学性质 |
| C、分子之间有间隙 |
| D、分子是由原子构成的 |
