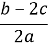题目内容
为了证明铁和硫反应产物中铁的化合价,下面是某同学设计的实验过程的一部分:
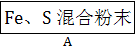

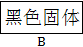
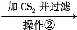

请回答下列问题:
(1)混合粉末A中硫粉过量的原因是
。
(2)反应在“惰气环境”中进行的原因是
。
(3)操作①用烧热的玻璃棒点触混合粉末,反应即可持续进行,说明
。
(4)操作②的作用是
。
(5)操作③稀硫酸煮沸的目的是
。
(6)为了证明产物中铁元素的价态,对D溶液的实验操作最好是
。
(1)防止因铁过量而使滤渣C中含铁粉与H2SO4反应,生成Fe2+干扰实验
(2)防止空气中的O2参与反应
(3)硫和铁的反应是放热反应
(4)除去混合物中的硫粉
(5)防止溶液中溶解的O2与Fe2+反应
(6)加入KSCN溶液,若不变红,再滴加氯水
【解析】
试题分析:铁和硫反应生成FeS,要验证产物中铁的化合价,必须排除Fe和Fe3+的干扰。硫粉过量的目的是保证Fe全部反应;加入CS2的目的是除去过量的硫粉,空气中的氧气能够将Fe2+氧化成Fe3+,所以反应要在“惰气环境”中进行,溶解滤渣的稀硫酸要先加热煮沸以排除其中所含氧气的影响。检验Fe2+或Fe3+,应用KSCN溶液和氯水。
考点:硫酸的制备和性质

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案下列有关实验操作、现象和解释或结论都正确的是
选项 | 操作 | 现象 | 解释或结论 |
A | 过量的Fe粉中加入稀HNO3,充分反应后,滴加KSCN溶液 | 溶液呈红色 | 稀HNO3将Fe氧化为Fe3+ |
B | Al箔插入稀HNO3中 | 无现象 | Al箔表面被稀HNO3氧化, 形成致密的氧化膜 |
C | 向某溶液中滴加稀NaOH溶液,将湿润 红色石蕊试纸置于试管口 | 试纸未变蓝 | 不能确定该溶液中是否含 有NH4+ |
D | 向紫色石蕊试液中通入SO2 | 溶液褪色 | SO2有漂白性 |
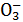 、Cl-B.K+、Na+、Br-、Cl-
、Cl-B.K+、Na+、Br-、Cl- 、HC
、HC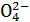
 的物质的量浓度(单位mol·L-1)为 ( )
的物质的量浓度(单位mol·L-1)为 ( ) B.
B.
 D.
D.