题目内容
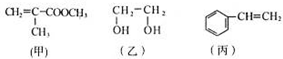 “神十”宇航员使用的氧气瓶是以聚酯玻璃钢为原料.如图甲、乙、丙三种物质是合成聚酯玻璃钢的基本原料.下列说法中,错误的是( )
“神十”宇航员使用的氧气瓶是以聚酯玻璃钢为原料.如图甲、乙、丙三种物质是合成聚酯玻璃钢的基本原料.下列说法中,错误的是( )| A、甲物质可以在引发剂作用下生成有机高分子化合物 |
| B、1mol乙物质可与2mol钠完全反应生成1mol氢气 |
| C、丙物质能够使酸性高锰酸钾溶液退色 |
| D、甲、乙、丙三种物质都可以发生加成反应 |
考点:有机物的结构和性质
专题:有机物的化学性质及推断
分析:A.甲含有碳碳双键,可发生加聚反应;
B.乙含有2个羟基,可与钠反应生成氢气;
C.丙含有碳碳双键,可发生氧化反应,
D.乙不含不饱和键,不能发生加成反应.
B.乙含有2个羟基,可与钠反应生成氢气;
C.丙含有碳碳双键,可发生氧化反应,
D.乙不含不饱和键,不能发生加成反应.
解答:
解:A.甲含有碳碳双键,可发生加聚反应生成有机高分子化合物,故A正确;
B.乙含有2个羟基,可与钠反应生成氢气,1mol乙物质可与2mol钠完全反应生成1mol氢气,故B正确;
C.丙含有碳碳双键,可发生氧化反应,故C正确,
D.乙不含不饱和键,不能发生加成反应,故D错误.
故选D.
B.乙含有2个羟基,可与钠反应生成氢气,1mol乙物质可与2mol钠完全反应生成1mol氢气,故B正确;
C.丙含有碳碳双键,可发生氧化反应,故C正确,
D.乙不含不饱和键,不能发生加成反应,故D错误.
故选D.
点评:本题考查有机物的结构和性质,为高考常见题型,侧重于学生的分析能力的考查,注意把握有机物的结构特点和官能团的性质,为解答该题的关键,难度不大.

练习册系列答案
相关题目
短周期主族元素X、Y、Z、W的原子序数依次增大,X的原子半径比Y的小,X与W同主族,Y、Z族序数之和为11,Z原子最外层电子数是内层电子总数的3倍.下列说法不正确的是( )
| A、元素Z、W的简单离子的电子层结构相同 |
| B、元素Y的简单气态氢化物的热稳定性比Z的弱 |
| C、由X、Y、Z三种元素形成化合物,其水溶液可能显碱性 |
| D、W、Z两种元素形成的化合物中肯定不含共价键 |
化学与环境、材料、信息、能源关系密切,下列说法错误的是( )
| A、半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是二氧化硅 |
| B、将“地沟油”制成肥皂,可以提高资源的利用率 |
| C、我国首艘航母“辽宁舰”上用于舰载机降落的拦阻索是特种钢缆,属于金属材料 |
| D、推广以植物秸秆为原料的综合利用技术,避免焚烧秸秆造成空气污染 |
下列实验过程和过程中涉及的离子反应方程式正确的是( )
| A、除去硫酸铜溶液中的硫酸亚铁以最终制备胆矾晶体:2Fe2++Cl2═2Fe3++2Cl- |
| B、Fe(OH)3与氢溴酸溶液混合:Fe(OH)3+3HBr═Fe3++3Br-+3H2O |
| C、用氨水吸收烟道气中的SO2:SO2+2NH3?H2O═2NH4++SO32-+H2O |
| D、醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+═Ca2++H2O+CO2↑ |
 甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是①CH3OH(g)+H2O(g)→CO2(g)+3H2(g)-49.0kJ
②CH3OH(g)+
| 1 |
| 2 |
下列说法正确的是( )
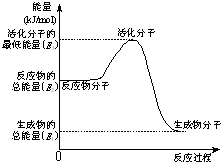
| A、上述图示的反应为吸热反应 |
| B、图中的能量变化如图所示,则Q=E3-E1 |
| C、H2燃烧能放出大量的热,故CH3OH转变成H2的过程必须吸收热量 |
| D、根据①②推知:在25℃,101kPa时,1mol CH3OH(g)完全燃烧生成CO2和H2O放出的热量应676.7kJ |
下列有关化学用语使用正确的是( )
A、羟基乙酸(HOCH2COOH)的缩聚物: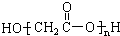 |
B、H2O2的分子结构模型示意图: |
| C、在CS2、PCl5中各原子最外层均能达到8电子的稳定结构 |
| D、淀粉和纤维素的实验式都为 CH2O |
下列离子反应方程式能正确表达相关反应的是( )
| A、在FeBr2溶液中通入足量氯气:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | ||||
B、用石墨电极电解氯化镁溶液:2Cl-+2H2O
| ||||
| C、向CaCl2溶液中通入CO2气体:Ca2++CO2+H2O═CaCO3↓+2H+ | ||||
| D、等物质的量浓度的小苏打溶液和石灰水按体积比3:2混合:3HCO3-+2Ca2++3OH-═2CaCO3↓+CO32-+3H2O |
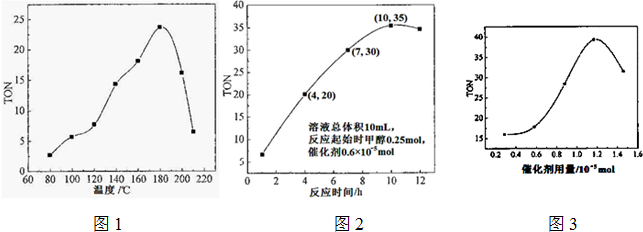
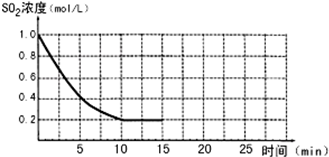 已知:2SO2(g)+O2(g)?2SO3(g);△H=-196kJ/mol,850K时,在2L固定容积的密闭容器中充入2mol SO2和2mol O2,10分钟后达到平衡,SO2浓度和时间关系如图.
已知:2SO2(g)+O2(g)?2SO3(g);△H=-196kJ/mol,850K时,在2L固定容积的密闭容器中充入2mol SO2和2mol O2,10分钟后达到平衡,SO2浓度和时间关系如图.