题目内容
14.粗CuO是将工业废铜、废铜合金等高温焙烧而成的,杂质主要是铁的氧化物及泥沙.以粗CuO为原料制备胆矾的主要流程如下:
经操作Ⅰ得到粗胆矾,操作Ⅲ得到精制胆矾.两步操作相同,具体包括蒸发浓缩、冷却结晶、过滤、洗涤、干燥等步骤.
已知:Fe3+、Fe2+、Cu2+转化为相应氢氧化物时,开始沉淀和沉淀完全时的pH如下表:
| Fe3+ | Fe2+ | Cu2+ | |
| 开始沉淀时的pH | 2.7 | 7.6 | 5.2 |
| 完全沉淀时的pH | 3.7 | 9.6 | 6.4 |
(2)写出加入3% H2O2后发生反应的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.(原溶液显酸性).
(3)加稀氨水调节pH应调至范围3.7~5.2.下列物质可用来替代稀氨水的是BC.(填字母)
A.NaOHB.Cu(OH)2C.CuOD.NaHCO3
(4)操作Ⅲ析出胆矾晶体后,溶液中还可能存在的溶质为CuSO4、H2SO4、(NH4)2SO4 或NH4HSO4.
(5)某学生用操作Ⅲ所得胆矾进行“硫酸铜晶体结晶水含量”的测定,数据记录如下表所示:
| 第一次实验 | 第二次实验 | |
| 坩埚质量(g) | 14.520 | 14.670 |
| 坩埚质量+晶体质量(g) | 17.020 | 18.350 |
| 第一次加热、冷却、称量(g) | 16.070 | 16.989 |
| 第二次加热、冷却、称量(g) | 16.070 | 16.988 |
A.加热前称量时坩埚未完全干燥B.该胆矾中含有受热不分解的杂质
C.加热后坩埚放在干燥器中冷却D.玻璃棒上沾有的固体未刮入坩埚.
分析 在粗CuO中加入硫酸生成硫酸铜、硫酸铁、硫酸亚铁等物质,经操作I得到粗胆矾,然后加入过氧化氢,将亚铁离子氧化为铁离子,使之在铜离子之前沉淀,加氨水调节pH值目的是让三价铁离子沉淀,但是铜离子不沉淀,然后调节溶液pH1~2之间可得到纯净的硫酸铜溶液,经蒸发浓缩、冷却结晶可得到胆矾,
(1)溶解时需要玻璃棒搅拌,过滤时需要玻璃棒引流;
(2)过氧化氢与Fe2+发生氧化还原反应;
(3)调节pH的范围应使Fe3+完全沉淀而Cu2+不生成沉淀,且尽量不引入新的杂质;
(4)因加入氨水,则可能生成(NH4)2SO4 或NH4HSO4;
(5)根据结晶水合物中,结晶水的质量=m(容器十晶体)-m(容器十无水硫酸铜),据化学方程式可以计算结晶水x的值,在测定中若被测样品中含有加热挥发的杂质或实验前容器中有水或玻璃棒上沾有的固体未刮入坩埚,都会造成测量结果偏高.
解答 解:在粗CuO中加入硫酸生成硫酸铜、硫酸铁、硫酸亚铁等物质,经操作I得到粗胆矾,然后加入过氧化氢,将亚铁离子氧化为铁离子,使之在铜离子之前沉淀,加氨水调节pH值目的是让三价铁离子沉淀,但是铜离子不沉淀,然后调节溶液pH1~2之间可得到纯净的硫酸铜溶液,经蒸发浓缩、冷却结晶可得到胆矾,
(1)溶解时需要玻璃棒搅拌,过滤时需要玻璃棒引流,故答案为:搅拌、引流;
(2)过氧化氢与Fe2+发生氧化还原反应,反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O,故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
(3)调节pH的范围应使Fe3+完全沉淀而Cu2+不生成沉淀,由表中数据可知应调节pH介于3.7~5.2之间,且尽量不引入新的杂质,则可用氢氧化铜、氧化铁或碳酸铜代替,不能够用氢氧化钠或碳酸氢钠,易引入硫酸钠杂质,
故答案为:3.7~5.2;BC;
(4)因加入氨水,则可能生成(NH4)2SO4 或NH4HSO4,故答案为:(NH4)2SO4 或NH4HSO4;
(5)由表中数据可知,由表格中的数据,第一次酸硫铜的质量为16.070g-14.520g=1.55g,水的质量:17.020g-16.070g=0.95g,
第二次酸硫铜的质量为:$\frac{16.988+16.989}{2}$g-14.670g=2.3185g,水的质量:18.350g-$\frac{16.988+16.989}{2}$g=1.3615g,
硫酸铜的平均质量为$\frac{1.55g+2.3185g}{2}$=1.934g,水的平均重量为$\frac{0.95g+1.3615g}{2}$=1.156g,
则n(CuSO4)=$\frac{1.934g}{160g/mol}$=0.012mol,n(H2O)=$\frac{1.156g}{18g/mol}$=0.0642mol,
则结晶水的个数为$\frac{0.0642}{0.012}$=5.352,
该生此次实验的相对误差=$\frac{5.352-5}{5.352}$×100%=+6.6%,
A.加热前称量时坩埚未完全干燥,加热后水挥发,导致水的质量测定结果偏大,故A正确;
B.该胆矾中含有受热不分解的杂质,会导致硫酸铜质量偏小,水的含量偏小,故B错误;
C.加热后坩埚放在干燥器中冷却,对实验没有影响,故C错误;
D.玻璃棒上沾有的固体未刮入坩埚,导致固体质量偏小,水的质量偏大,故D正确.
故答案为:已达恒重;+6.6%;AD.
点评 本题考查物质的制备实验方案的设计,侧重于学生的分析能力、实验能力和计算能力的考查,为高考常见题型,注意根据流程图把握实验的原理和操作方法,难度不大,易错点为(5),注意把握误差的计算方法,从题目本身对学生的实验能力要求较高,但此题实际上就来源于课本的学生实验,只要学生认真的去操作过、体验过、思考过,就会觉得很熟悉、很简单.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 标准状况下,22.4LH2O含有的分子数为1 NA | |
| B. | 常温常压下,10.6g Na2CO3含有的Na+离子数为0.2 NA | |
| C. | 通常状况下,1 NA 个CO2分子占有的体积为22.4L | |
| D. | 物质的量浓度为0.5mol•/L的MgCl2溶液中,含有Cl- 个数为1 NA |
| A. | ${\;}_{22}^{48}$Ti和${\;}_{22}^{50}$Ti的质量数不同,属于两种元素 | |
| B. | ${\;}_{1}^{1}$H2、${\;}_{1}^{2}$H2、H2互为同位素 | |
| C. | 14462Sm其原子核内中子数和质子数都是62 | |
| D. | O2和O3互为同素异形体 |
| A. | 1mol NH5中含有5NA个N-H键(NA为阿伏加德罗常数) | |
| B. | NH5中既有共价键,又有离子键 | |
| C. | NH5的电子式为: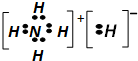 | |
| D. | 与水反应时,水作氧化剂,生成1mol氢气,转移2mol电子 |
| A. | 氨水 | B. | 氢氧化铁胶体 | C. | 混有冰的水 | D. | 石灰石 |
| A. | 25 mL 0.2mol/L的NaCl溶液 | B. | 100mL 0.1 mol/L的NaCl溶液 | ||
| C. | 25 mL 0.2 mol/L的Na2SO4溶液 | D. | 10 mL 0.5 mol/L的Na2CO3溶液 |
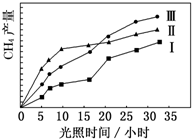 利用光能和光催化剂,可将 CO2 和 H2O(g)转化为 CH4 和 O2.紫外光照射时,在不同催化剂(Ⅰ,Ⅱ,Ⅲ)作用下,CH4产量随光照时间的变化如图所示.
利用光能和光催化剂,可将 CO2 和 H2O(g)转化为 CH4 和 O2.紫外光照射时,在不同催化剂(Ⅰ,Ⅱ,Ⅲ)作用下,CH4产量随光照时间的变化如图所示.