题目内容
下列有关叙述中正确的是( )
| A、碳酸钙在水里的溶解度很小,所以碳酸钙是弱电解质 |
| B、NH3的水溶液导电,所以NH3是电解质 |
| C、强电解质在水溶液中的电离过程是不可逆的 |
| D、强电解质的水溶液导电能力一定比弱电解质的水溶液导电能力强 |
考点:强电解质和弱电解质的概念,电解质与非电解质
专题:电离平衡与溶液的pH专题
分析:A、碳酸钙溶于水的部分完全电离;
B、氨气分子不能自身电离出自由移动的离子;
C、强电解质在水溶液中完全电离;
D、电解质溶液的导电能力取决于离子浓度和离子所带电荷.
B、氨气分子不能自身电离出自由移动的离子;
C、强电解质在水溶液中完全电离;
D、电解质溶液的导电能力取决于离子浓度和离子所带电荷.
解答:
解:A、碳酸钙溶于水的部分完全电离,属于强电解质,故A错误;
B、氨气分子不能自身电离出自由移动的离子,氨气属于非电解质,故B错误;
C、强电解质在水溶液中完全电离,其电离过程不可逆,故C正确;
D、电解质溶液的导电能力取决于离子浓度和离子所带电荷,故D错误;
故选C.
B、氨气分子不能自身电离出自由移动的离子,氨气属于非电解质,故B错误;
C、强电解质在水溶液中完全电离,其电离过程不可逆,故C正确;
D、电解质溶液的导电能力取决于离子浓度和离子所带电荷,故D错误;
故选C.
点评:本题考查了电解质与非电解质、强电解质与弱电解质,题目难度不大,注意掌握概念的外延和内涵、电解质溶液的导电能力取决于离子浓度和离子所带电荷,并不是强电解质的水溶液导电能力一定比弱电解质的水溶液导电能力强.

练习册系列答案
相关题目
将SO2气体通入BaCl2溶液至饱和,无沉淀生成,再通入另一种气体仍没有沉淀生成,则第二次通入的气体可能是下列气体中的( )
①NO2 ②CO2③Cl2 ④HCl ⑤NH3 ⑥H2S.
①NO2 ②CO2③Cl2 ④HCl ⑤NH3 ⑥H2S.
| A、②④⑥ | B、①⑤⑥ |
| C、②④ | D、②③⑤ |
下列各物质的名称正确的是( )
| A、1,2-二甲基丁烷 |
| B、2,3,3-三甲基-2-丁烯 |
| C、3,4,4-三甲基-1-戊炔 |
| D、2,3-二甲基苯 |
同温同压下,等质量的O2和CO2相比较,下列叙述正确的是( )
| A、体积比为8:1 |
| B、分子个数之比为11:12 |
| C、物质的量之比为11:8 |
| D、原子个数之比为11:12 |
饱和的H2S溶液中,微粒浓度最大的是( )
| A、H+ |
| B、HS- |
| C、OH- |
| D、H2S |
下列关于Na2O和Na2O2的叙述正确的是( )
| A、都是白色固体 |
| B、都能和水反应形成强碱溶液 |
| C、都是碱性氧化物 |
| D、都是强氧化剂 |
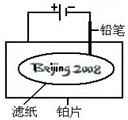 某学生设计了如图所示的“黑笔写红字”的趣味实验.滤纸上先用NaCl和无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹--“Beijing2008”. 据此,下列叙述不正确的是( )
某学生设计了如图所示的“黑笔写红字”的趣味实验.滤纸上先用NaCl和无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹--“Beijing2008”. 据此,下列叙述不正确的是( )| A、铅笔作阴极:电极反应为:2H++2e-=H2↑ | ||||
| B、铂片作阳极:电极反应为:2Cl--2e-=Cl2↑ | ||||
| C、铅笔与滤纸接触处有少量Cl2逸出 | ||||
D、上述反应总的离子方程式可表示为2Cl-+2H2O
|
下列说法正确的是( )
| A、海水中蕴含的元素有80多种,其中Mg、Br、I在海水中的总储量分别约为1.8×1015t、1×1014t、8×1010t.由于海水中镁的储量很大,工业上常以海水为原料提取镁,因此,镁元素被称为“海洋元素” |
| B、活泼金属元素的氧化物一定是碱性氧化物,非金属元素的氧化物一定是酸性氧化物 |
| C、氢氧化铁溶胶、甘油与乙醇的混合液、含PM2.5的大气均具有丁达尔效应 |
| D、绿色化学期望利用化学原理从源头消除污染,在化学过程中充分利用原料,实现零排放 |
下列有关实验的操作正确的是( )
| A、容量瓶、量筒和滴定管上都标有使用温度,量筒、容量瓶无“0”刻度,滴定管有“0”刻度;使用时滴定管水洗后还需润洗,但容量瓶水洗后不用润洗 |
| B、检验某溶液是否含有SO42-时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸 |
| C、为观察Mg条在CO2气体中的燃烧,在一个底部铺有少量玻璃棉的集气瓶中收集满 CO2气体,取一小段除去表面氧化膜的Mg条用坩埚钳夹持点燃后迅速投入上述集气瓶底部 |
| D、用干燥且洁净的玻璃棒蘸取NaClO溶液,滴到放在表面皿上的pH试纸上测pH值 |