题目内容
已知:CH4(g)+CO2(g)=2CO(g)+2H2(g);△H=+247.4kJ?mol-1.CH4(g)+H2O(g)=CO(g)+3H2(g);△H=+206.2kJ?mol-1.则CH4(g)+2H2O(g)=CO2(g)+4H2(g)的△H为( )
| A、-41.2kJ?mol-1 |
| B、+165.0kJ?mol-1 |
| C、-288.6kJ?mol-1 |
| D、+453.6kJ?mol-1 |
考点:用盖斯定律进行有关反应热的计算
专题:
分析:依据热化学方程式和盖斯定律计算得到CH4(g)+2H2O(g)=CO2(g)+4H2(g)的△H.
解答:
解:①CH4(g)+CO2(g)=2CO(g)+2H2(g);△H=+247.4kJ?mol-1
②CH4(g)+H2O(g)=CO(g)+3H2(g);△H=+206.2kJ?mol-1;
结合盖斯定律②×2-①得到CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为:CH4(g)+2H2O(g)=CO2(g)+4H2(g)△H=+165.0kJ?mol-1,
故选B.
②CH4(g)+H2O(g)=CO(g)+3H2(g);△H=+206.2kJ?mol-1;
结合盖斯定律②×2-①得到CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为:CH4(g)+2H2O(g)=CO2(g)+4H2(g)△H=+165.0kJ?mol-1,
故选B.
点评:本题考查了反应热的计算,侧重于盖斯定律在计算中的应用的考查,掌握盖斯定律的原理是关键,题目较简单.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列常见物质的分类不正确的是( )
| A、CO2是酸性氧化物 |
| B、氨水是混合物 |
| C、冰醋酸是电解质 |
| D、纯碱是碱 |
已知R2+核外有a个电子,b个中子.表示R原子符号正确的是( )
| A、R | ||
B、
| ||
C、
| ||
D、
|
下列说法错误的是( )
| A、淀粉、油脂、蛋白质都能水解,但水解产物不同 |
| B、煤油可由石油分馏获得,可用作燃料和保存少量金属钠 |
| C、植物油和裂化汽油都可以使溴水褪色 |
| D、使用生物酶降解生活废水中的有机物,使用填埋法处理未经分类的生活垃圾 |
下列溶液在空气中加热蒸干并灼烧后,能得到相应溶质固体的是( )
| A、FeCl3 |
| B、KHCO3 |
| C、Fe2(SO4)3 |
| D、FeSO4 |
下列离子方程式正确的是( )
| A、稀硝酸与氢氧化钾溶液反应 H++OH-=H2O |
| B、铝与稀盐酸反应 Al+2H+=Al3++H2↑ |
| C、三氯化铁溶液与氢氧化钠溶液反应 FeCl3+3OH-=Fe(OH)3↓+3Cl- |
| D、足量二氧化碳与澄清石灰水反应 CO2+2OH-=CO32-+H2O |
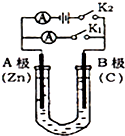 如图所示,U形管内盛有100mL的溶液,按要求回答下列问题:
如图所示,U形管内盛有100mL的溶液,按要求回答下列问题: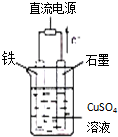 (1)已知298K时,1molC2H6在氧气中完全燃烧生成二氧化碳和液态水,利用该反应设计一个燃料电池:用氢氧化钾溶液做电解质溶液,用多孔石墨做电极,在电极上分别充入乙烷和氧气.写出负极的电极反应式
(1)已知298K时,1molC2H6在氧气中完全燃烧生成二氧化碳和液态水,利用该反应设计一个燃料电池:用氢氧化钾溶液做电解质溶液,用多孔石墨做电极,在电极上分别充入乙烷和氧气.写出负极的电极反应式