题目内容
20. 已知:2X(g)+Y(g)?a Z(g),在T1温度下,体积为2L的密闭容器中,充入6mol X和2mol Y.根据图示回答:
已知:2X(g)+Y(g)?a Z(g),在T1温度下,体积为2L的密闭容器中,充入6mol X和2mol Y.根据图示回答:(1)a=1;用Y的浓度变化表示从反应开始到平衡时的平均反应速率为0.075mol/(L•min).
(2)平衡时,Y在混合物中的物质的量分数是10%.
(3)其他条件不变时,下列措施可以提高Y的转化率的是B(选填字母).
A.使用适当的催化剂 B.分离出Z C.增大容器体积.
分析 (1)各物质的化学计量数之比等于浓度变化量之比;根据反应速率v=$\frac{△c}{△t}$计算;
(2)根据Y在混合物中的物质的量分数=$\frac{n(Y)}{n(总)}$计算;
(3)可以提高Y的转化率,平衡正向进行.
解答 解:(1)在体积为2L的密闭容器中充入6molX和2molY,X、Y的起始浓度分别为3mol/L、1mol/L,平衡时X、Y、Z浓度变化之比为△c(x):(1.00mol/L-0.25mol/l):0.75mol/L=2:1:1,故a=1,△c(x)=1.5mol/L,用Y的浓度变化表示从反应开始到平衡时的平均反应速率为$\frac{△c}{△t}$=$\frac{0.75mol/L}{10min}$=0.075mol/L,
故答案为:1;0.075mol/(L•min);
(2)平衡时n(X)=(3mol/L-1.5mol/L)×2L=3mol,n(Y)=0.25mol/L×2L=0.5mol,n(Z)=0.75mol/L×2L=1.5mol,则Y在混合物中的物质的量分数=$\frac{n(Y)}{n(总)}$=$\frac{0.5mol}{3mol+0.5mol+1.5mol}$×100%=10%,
故答案为:10%;
(3)反应2X(g)+Y(g)?Z(g),提高Y的转化率,即使平衡正向移动,
A.催化剂不影响平衡平衡,故A错误;
B.分离出Z,平衡正向移动,Y转化率增大,故B正确;
C.增大容器体积,压强减小平衡逆向移动,Y转化率减小,故C错误;
故答案为:B.
点评 本题考查了反应速率的计算,化学平衡影响因素,平衡状态的判断、图象分析计算等知识点,综合性较强,难度中等.

练习册系列答案
 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
16.若用NA表示阿伏加德罗常数的值,下列叙述不正确的是( )
| A. | 1mol BrCl与H2O完全反应生成氯化氢和次溴酸,转移的电子数为NA | |
| B. | 锌与一定浓度的浓硫酸反应,产生标准状况下SO2和H2的混合气体22.4L,锌失去电子数为2NA | |
| C. | 常温常压下,20g D2O含有的原子总数为3NA | |
| D. | 标准状况下,44.8L NO与22.4L O2混合气体中分子总数小于2NA |
8.下列说法正确的是( )
| A. | 乙烯能使溴水、酸性高锰酸钾溶液褪色,其反应类型相同 | |
| B. | 某烷烃R的相对分子质量为86,其氯代物只有2种,则R的名称一定为2,3-二甲基丁烷 | |
| C. | 若甲烷与氯气以物质的量之比1:3混合,在光照下得到的产物只有CHCl3 | |
| D. | 在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH |
15.手性分子是指在分子结构 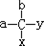 中,当a、b、x、y为彼此互不相同的原子或原子团时,称此分子为手性分子,中心碳原子为手性碳原子.下列分子中指定的碳原子(用*标记)不属于手性碳原子的是( )
中,当a、b、x、y为彼此互不相同的原子或原子团时,称此分子为手性分子,中心碳原子为手性碳原子.下列分子中指定的碳原子(用*标记)不属于手性碳原子的是( )
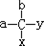 中,当a、b、x、y为彼此互不相同的原子或原子团时,称此分子为手性分子,中心碳原子为手性碳原子.下列分子中指定的碳原子(用*标记)不属于手性碳原子的是( )
中,当a、b、x、y为彼此互不相同的原子或原子团时,称此分子为手性分子,中心碳原子为手性碳原子.下列分子中指定的碳原子(用*标记)不属于手性碳原子的是( )| A. | 苹果酸: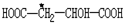 | B. | 丙氨酸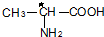 | C. | 葡萄糖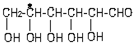 | D. | 甘油醛 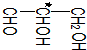 |
5.用如图所示装置能达到有关实验目的是( )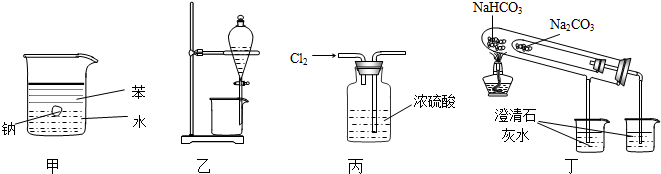

| A. | 用甲图装置证明密度ρ(苯)<ρ(钠)<ρ(水) | |
| B. | 用乙图装置分离酒精和四氯化碳 | |
| C. | 用丙图装置干燥Cl2 | |
| D. | 用丁图装置比较NaHCO3和Na2CO3的热稳定性 |
12.下列反应的离子方程式书写正确的是( )
| A. | 硫酸和氯氧化钡溶液反应:Ba2++SO42-═BaSO4↓ | |
| B. | 碳酸钠与盐酸反应:Na2CO3+2H+═2Na++CO2↑+H2O | |
| C. | Ca(NO3)2溶液和Na2CO3溶液混合:Ca2++CO32-═CaCO3↓ | |
| D. | 铁钉放入硫酸铁溶液中:Fe+Fe3+═2Fe2+ |
9.将5.6gFe投入浓硝酸中,产生红棕色气体A,把所得溶液减压蒸干,得到20gFe(NO3)2和Fe(NO3)3的混合物,将该固体在高温下加热,得到红棕色的Fe2O3和气体B,A、B气体混合通入足量水中,在标准状况下剩余气体的体积为( )
| A. | 1120mL | B. | 2240mL | C. | 3360mL | D. | 4480mL |
10.反应N2(g)+O2(g)?2NO(g)在密闭容器中进行,下列条件不能改变该反应的速率的是( )
| A. | 缩小体积使压强增大 | B. | 体积不变充入N2使压强增大 | ||
| C. | 体积不变充入氦气使压强增大 | D. | 压强不变充入N2使体积增大 |