题目内容
17.蓄电池是典型的可充型电池,它的正负极格板是惰性材料,电池总反应式为:Pb+PbO2+4H++2SO42-$?_{充电}^{放电}$2PbSO4+2H2O请回答下列问题:已知硫酸铅不溶于水,放电时,该电池的负极反应为 Pb-2e-+SO42-═PbSO4,(1)则正极的电极反应式是PbO2+2e-+4H++SO42-=PbSO4+2H2O;
(2)当外电路通过1mol电子时,理论上负极板的质量增加48g.电解质溶液中溶质减少的物质的量为1mol.
分析 (1)根据电池总反应Pb+PbO2+4H++2SO42-$?_{充电}^{放电}$2PbSO4+2H2O可知负极铅失电子发生氧化反应,电极反应为Pb-2e-+SO42-=PbSO4 ,正极二氧化铅得电子发生还原反应,电极反应为PbO2+2e-+4H++2SO42-=PbSO4+2H2O;
(2)负极板增加的质量等于负极参加反应的硫酸根的质量,根据电池总反应计算消耗硫酸的物质的量.
解答 解:(1)二氧化铅作正极得电子发生还原反应,电极反应式为PbO2+2e-+4H++SO42-=PbSO4+2H2O,
故答案为:PbO2+2e-+4H++SO42-=PbSO4+2H2O;
(2)铅作负极,电极反应式为Pb-2e-+SO42-=PbSO4,当外电路通过1mol电子时,负极生成0.5mol PbSO4,则负极板的质量增加0.5mol×96g/mol=48g;
根据电池总反应Pb+PbO2+4H++2SO42-$?_{充电}^{放电}$2PbSO4+2H2O可知有2mol硫酸参加反应时,转移电子的物质的量是2mol,所以当外电路通过1mol电子时,消耗硫酸的物质的量是1mol,
故答案为:48;1mol.
点评 本题考查了原电池原理,会根据电池反应式及元素化合价变化书写正负极电极反应式,再结合各个物理量之间的关系式进行计算,注意:负极上生成难溶性的硫酸铅导致负极质量增加,题目难度不大.

练习册系列答案
相关题目
5.表是某城市空气质量每周公报的部分内容.下列选项中不会对表中3个空气质量指标产生影响的是( )
| 项目 | 空气污染指数(API) | 空气质量级别 | 空气质量描述 |
| 总悬浮颗粒 | 52 | Ⅱ | 良 |
| 二氧化硫 | 7 | I | 优 |
| 二氧化氮 | 24 | I | 优 |
| A. | 用煤和石油产品作燃料 | B. | 汽车排放的尾气 | ||
| C. | 使用含磷洗衣粉 | D. | 焚烧垃圾 |
12.从键长的角度来判断下列共价键中最稳定的是( )
| A. | H-F | B. | H-N | C. | H-C | D. | H-S |
2.关于溶液的下列说法正确的是( )
| A. | 等体积、对物质的量浓度的NaX和弱酸HX混合后的溶液中:C(Na+)>c(HX)>c(X-)>c(H+)>c(OH-) | |
| B. | 等物质的量浓度的下列溶液:①H2CO3②Na2CO3③NaHCO3④(NH4)2CO3中c(CO32-)的大小关系为:②>④>③>① | |
| C. | 往0.1mol/L CH3COOH溶液中通入少量HCl,醋酸的电离平衡向逆反应方向移动,且溶液中$\frac{c(C{H}_{3}COOH)}{c({H}^{+})•c(C{H}_{3}CO{O}^{-})}$增大 | |
| D. | Na2CO3溶液中,2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) |
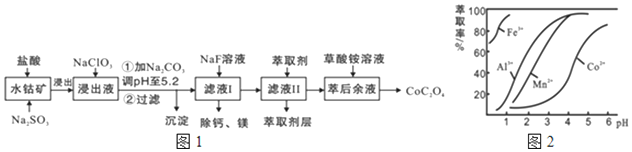
9.草酸钴用途广泛,可用于指示剂和催化剂的制备.一种利用水钴矿制取草酸钴晶体(CoC2O4?2H2O)工艺流程如图1:
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
(1)浸出过程中加入Na2SO3的 离子方程式为2Co3++SO32-+H2O=2Co2++SO42-+2H+
(2)NaClO3的作用是将Fe2+氧化为Fe3+; 调PH至5.2,沉淀的主要成分为Al(OH)3、Fe(OH)3
(3)萃取剂对金属离子的萃取率与pH的关系如图2所示.滤液Ⅱ中加入萃取剂的作用是除去Mn2+;使用萃取剂适宜的pH是B
A.接近2.0 B.接近3.0 C.接近5.0
(4)除钙、镁是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀,已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10.当加入过量NaF后,所得滤液c(Mg2+):c(Ca2+)=0.7.
(5)已知含钴废料中含Co2O3质量分数为a%,若取mkg该含钴废料按照上述流程,理论上最多能制得草酸钴晶体的质量为$\frac{1830ma}{83}$或16.6mag.

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 完全沉淀的PH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(2)NaClO3的作用是将Fe2+氧化为Fe3+; 调PH至5.2,沉淀的主要成分为Al(OH)3、Fe(OH)3
(3)萃取剂对金属离子的萃取率与pH的关系如图2所示.滤液Ⅱ中加入萃取剂的作用是除去Mn2+;使用萃取剂适宜的pH是B
A.接近2.0 B.接近3.0 C.接近5.0
(4)除钙、镁是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀,已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10.当加入过量NaF后,所得滤液c(Mg2+):c(Ca2+)=0.7.
(5)已知含钴废料中含Co2O3质量分数为a%,若取mkg该含钴废料按照上述流程,理论上最多能制得草酸钴晶体的质量为$\frac{1830ma}{83}$或16.6mag.
6.下列描述中正确的是( )
| A. | CS2为V形的极性分子 | |
| B. | ClO3-的空间构型为平面三角形 | |
| C. | SF6中所有原子均满足8电子稳定结构 | |
| D. | SiF4和SO32-的中心原子均为印sp3杂化 |
 .
.