题目内容
含NO3-的工业废水会造成水体富营养化,可利用如下反应将其转化为无毒、无污染的N2:A1+口+口→口十口+口,反应中涉及到的另外3种微粒是H2O、A1(OH)3、OH-.下列说法正确的是( )
| A、反应中的Al被还原,NO3-是还原剂 |
| B、三种反应物分别是Al、NO3-和OH- |
| C、若有1 mol Al参加反应,则有0.6 mol NO3-被还原 |
| D、随着反应的进行,溶液的碱性逐渐减弱 |
考点:氧化还原反应
专题:
分析:A1与NO3-发生氧化还原反应,Al转化为A1(OH)3化合价升高失电子,NO3-转化为N2化合价降低得电子,则发生的反应为10Al+18H2O+6NO3-=10Al(OH)3↓+3N2↑+6OH-,据此分析.
解答:
解:A.A1与NO3-发生氧化还原反应,Al转化为A1(OH)3化合价升高失电子,则Al为还原剂,NO3-转化为N2化合价降低得电子,则NO3-为氧化剂,故A错误;
B.反应为10Al+18H2O+6NO3-=10Al(OH)3↓+3N2↑+6OH-.则OH-为生成物,故B错误;
C.若有1 mol Al参加反应,转移电子为3mol,则有0.6 mol NO3-被还原,故C正确;
D.由于有OH-生成,所以随着反应的进行,溶液的碱性逐渐增强,故D错误.
故选C.
B.反应为10Al+18H2O+6NO3-=10Al(OH)3↓+3N2↑+6OH-.则OH-为生成物,故B错误;
C.若有1 mol Al参加反应,转移电子为3mol,则有0.6 mol NO3-被还原,故C正确;
D.由于有OH-生成,所以随着反应的进行,溶液的碱性逐渐增强,故D错误.
故选C.
点评:本题考查了氧化还原反应,题目涉及反应物和生成物的判断、方程式的书写等,注意根据化合价的变化分析,题目难度不大.

练习册系列答案
相关题目
用18mol/L H2SO4溶液和100mL容量瓶配置1.8mol/L H2SO4溶液,下列有关说法正确的是( )
| A、将10mL 18mol/L H2SO4溶液加入盛有90mL水的容量瓶中 |
| B、将10mL 18mol/L H2SO4溶液加入容量瓶中,加水至刻度线 |
| C、加水时不慎超过刻度线,立即用胶头滴管吸出多余液体 |
| D、定容时仰视刻度线,配置的溶液浓度偏小 |
下列反应的离子方程式正确的是( )
| A、向浓度均为0.1 mol?L-1的KNO3和KHSO4的混合溶液中加入铜片:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O |
| B、向Na2CO3浴液中逐滴加入少量稀盐酸:CO32-+2H+═H2O+CO2↑ |
| C、二氧化硫通人氯化铁溶液中:2Fe3++SO2+2H2O═2Fe2++4H++SO42- |
| D、在FeI2溶液中滴少量溴水:2Fe2++Br2═2Fe3++2Br- |
据美国《科学》杂志报道,外太空的某一星球的大气层中,含有大量的CH2=CHOH,此物质常温时为液体,它很容易转化成CH3CHO,化学方程式为CH2=CHOH?CH3CHO;已知△H<0.据此你认为下列说法中错误的是( )
| A、该星球表面温度很高 |
| B、该星球表面温度很低 |
| C、该反应为放热反应 |
| D、高温下稳定性CH2=CHOH>CH3CHO |
当光束通过下列分散系时,能观察到丁达尔效应的是( )
| A、盐酸 | B、氢氧化铁胶体 |
| C、氯化钠溶液 | D、硫酸铜溶液 |
用NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A、标准状况下,1 mol CO2和CO的混合气中含有的氧原子数为1.5NA |
| B、常温常压下,33.6 L 氯化氢气体中含有的分子数为1.5NA |
| C、12g Mg与足量二氧化碳反应转移的电子数为NA |
| D、1 mol?L-1 CuCl2溶液中含有的氯离子数为2NA |
下列过程没有发生化学反应的是( )
| A、用活性炭去除冰箱中的异味 |
| B、用热碱水清除炊具上残留的油渍 |
| C、用浸泡过高锰酸钾溶液的砖头储存水果 |
| D、用含硅胶、铁粉的透气小袋与食品一起密封包装 |
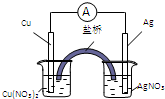 用铜片、银片、Cu(NO3)2溶液、AgNO3溶液、导线和盐桥(盛有KNO3琼脂的U型管)构成一个原电池.以下有关该原电池的叙述正确的是
用铜片、银片、Cu(NO3)2溶液、AgNO3溶液、导线和盐桥(盛有KNO3琼脂的U型管)构成一个原电池.以下有关该原电池的叙述正确的是