题目内容
4.在甲乙两烧杯溶液中,分别含有大量的Cu2+、K+、H+、Cl-、CO32-、OH-六种离子中的三种,已知乙烧杯中的溶液呈蓝色,则乙烧杯的溶液中大量存在的离子是( )| A. | Cu2+、H+、Cl- | B. | Cl-、CO32-、OH- | C. | K+、OH-、CO32- | D. | K+、H+、Cl- |
分析 乙烧杯中的溶液呈蓝色,则一定含Cu2+,与Cu2+结合生成沉淀的离子CO32-、OH-一定在甲中,由电荷守恒可知乙中阴离子一定为Cl-,以此来解答.
解答 解:乙烧杯中的溶液呈蓝色,则一定含Cu2+,与Cu2+结合生成沉淀的离子CO32-、OH-一定在甲中,由电荷守恒可知乙中阴离子一定为Cl-,
由电荷守恒及离子共存可知,甲中阳离子应为K+,
则甲烧杯的溶液中大量存在的离子是K+、OH-、CO32-,
乙烧杯的溶液中大量存在的离子是Cu2+、H+、Cl-,
故选A.
点评 本题考查离子的共存,为高频考点,把握乙烧杯中的溶液呈蓝色为解答的突破口,注意离子之间的反应及电荷守恒应用,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.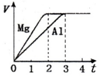 镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系
如图.反应中镁和铝的( )
 镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图.反应中镁和铝的( )
| A. | 物质的量之比为3:2 | B. | 质量之比为2:3 | ||
| C. | 摩尔质量之比为2:3 | D. | 反应速率之比为3:2 |
15.BaSO4的分子量为233,Ksp=1.0×10-10,把1.0mmol的BaSO4配成10dm3溶液,BaSO4没有溶解的量是( )
| A. | 0.0021g | B. | 0.021g | C. | 0.21g | D. | 2.1g |
12.下列有机物名称正确的是( )
| A. | 2,2,3-三甲基丁烷 | B. | 2-乙基戊烷 | ||
| C. | 2-甲基-1-丁炔 | D. | 2,2-二甲基-1-丁烯 |
19.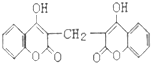 化学家从腐败草料中提取出双香豆素,结构简式如图.1mol双香豆素与NaOH溶液反应,最多可消耗NaOH的物质的量是( )
化学家从腐败草料中提取出双香豆素,结构简式如图.1mol双香豆素与NaOH溶液反应,最多可消耗NaOH的物质的量是( )
 化学家从腐败草料中提取出双香豆素,结构简式如图.1mol双香豆素与NaOH溶液反应,最多可消耗NaOH的物质的量是( )
化学家从腐败草料中提取出双香豆素,结构简式如图.1mol双香豆素与NaOH溶液反应,最多可消耗NaOH的物质的量是( )| A. | 4 mol | B. | 5mol | C. | 6 mol | D. | 8mol |
16.下列离子方程式书写不正确的是( )
| A. | 少量Mg(OH)2固体可溶于较浓的NH4Cl溶液中:Mg(OH)2+2NH4+═Mg2++2NH3•H2O | |
| B. | 在CuSO4溶液中加入PbS,可转变为铜蓝(CuS):Cu2++PbS═Pb2++CuS | |
| C. | 向NH4Al(SO4)2溶液中滴加Ba(OH)2溶液至SO42-沉淀完全:2Al3++3SO42-+3Ba2++6OH-═3BaSO4↓+2Al(OH)3↓ | |
| D. | 向Na2S2O3溶液中滴加稀硫酸,溶液变混浊:S2O32-+2H+═S↓+SO2↑+H2O |
14.下列物质中,溶于水且能发生电离的是( )
| A. | 硫酸钡 | B. | Cu | C. | NaCl | D. | 蔗糖 |