题目内容
硫代硫酸钠(Na2S2O3)与稀H2SO4溶液作用时,发生如下反应:Na2S2O3+H2SO4=Na2SO4+SO2+S↓+H2O,下列化学反应速率最大的是( )
| A、0.1mol/L Na2S2O3和0.1mol/L H2SO4溶液各5mL,加水5mL反应温度10℃ |
| B、0.1mol/L Na2S2O3和0.1mol/L H2SO4溶液各5mL,加水10mL反应温度10℃ |
| C、0.1mol/L Na2S2O3和0.1mol/L H2SO4溶液各5mL,加水10mL反应温度30℃ |
| D、0.2mol/L Na2S2O3和0.1mol/L H2SO4溶液各5mL,加水10mL反应温度30℃ |
考点:化学反应速率的影响因素
专题:
分析:参加反应的物质的浓度越大,反应速率越大,反应的温度越高,反应速率越大,并且温度对反应速率影响更大,根据以上方面进行分析判断.
解答:
解:反应温度对反应速率影响较大,由于浓度相差不大,所以首先比较反应温度高低,C、D选项中的反应温度高于A、B选项的温度,所以C、D的反应速率大于A、B的反应速率,C中的硫代硫酸钠的浓度小于D中的浓度,故反应速率D的大于C的,
故选D.
故选D.
点评:本题考查了影响反应速率大小的因素,注意温度对反应速率的影响更加明显,本题难度不大.

练习册系列答案
相关题目
通常用来衡量一个国家的石油化学工业发展水平标志的是( )
| A、石油产量 |
| B、乙烯的产量 |
| C、合成纤维的产量 |
| D、硫酸的产量 |
下列醇中既能发生消去反应,又能被氧化为酮的是( )
①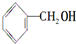 ②
② ③CH3OH④
③CH3OH④ ⑤
⑤ ⑥
⑥
①
 ②
② ③CH3OH④
③CH3OH④ ⑤
⑤ ⑥
⑥
| A、①④⑤ | B、②④⑥ |
| C、②⑥ | D、①②⑥ |
下图表示4-溴-1-环己醇所发生的4个不同反应(反应条件略去),产物含有二种官能团的反应是(


| A、②③ | B、①④ |
| C、①②④ | D、①②③④ |
为探究锌与稀硫酸的反应速率(以v(H2)表示),向反应混合液中加入某些物质,下列判断正确的是( )
| A、加入NH4HSO4固体,v(H2)增大 |
| B、加入少量水,v(H2)不变 |
| C、加入CH3COONa固体,v(H2)减小 |
| D、滴加少量CuSO4溶液,v(H2)减小 |
下列有机物命名正确的是( )
| A、3-甲基-2-戊炔 |
| B、3-乙基-1-丁烯 |
| C、2-甲基-1-丙醇 |
| D、3,4,4-三甲基己烷 |
物质的量的单位是( )
| A、mol |
| B、g?mol-1 |
| C、mol?L-1 |
| D、mol?L-1?s-1 |


 用铜片、锌片和200mL稀H2SO4等组成原电池(如图).若整个实验过程有6.5g锌溶解,此时H2SO4恰好全部用完.回答下列问题:
用铜片、锌片和200mL稀H2SO4等组成原电池(如图).若整个实验过程有6.5g锌溶解,此时H2SO4恰好全部用完.回答下列问题: