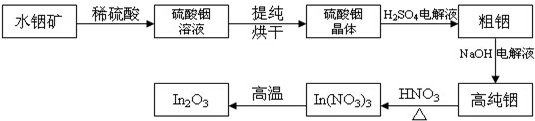
题目内容
12.用活性炭还原法可以处理氮氧化物,T℃时,向容积为1L的密闭容器中加入0.10molNO气体和2.03mol炭粉,发生反应:C(s)+2NO(g)═N2(g)+CO2(g)△H>0.2min后反应达到平衡,测得N2为0.03mol,下列有关说法错误的是( )| A. | 2min内,用NO表示的该反应的平均速度v(NO)=0.03mol•L-1•min-1 | |
| B. | 容器内混合气体密度保持不变可以说明反应达到平衡状态 | |
| C. | T℃时,该反应的平衡常数K=$\frac{9}{32}$ | |
| D. | 升高温度,可以提高反应速率和NO的转化率 |
分析 向容积为1L的密闭容器中加入0.10molNO气体和2.03mol炭粉,发生反应:C(s)+2NO(g)═N2(g)+CO2(g)△H>0.2min后反应达到平衡,测得N2为0.03mol,则消耗0.06molNO,则
C(s)+2NO(g)═N2(g)+CO2(g)
起始(mol)2.03 0.10 0 0
转化(mol)0.03 0.06 0.03 0.03
平衡(mol)2.00 0.04 0.03 0.03
结合方程式以及化学平衡的影响因素解答该题.
解答 解:向容积为1L的密闭容器中加入0.10molNO气体和2.03mol炭粉,发生反应:C(s)+2NO(g)═N2(g)+CO2(g)△H>0.2min后反应达到平衡,测得N2为0.03mol,则消耗0.06molNO,则
C(s)+2NO(g)═N2(g)+CO2(g)
起始(mol)2.03 0.10 0 0
转化(mol)0.03 0.06 0.03 0.03
平衡(mol)2.00 0.04 0.03 0.03
A.2min内,用NO表示的该反应的平均速度v(NO)=$\frac{\frac{0.06mol}{1L}}{2min}$=0.03mol•L-1•min-1,故A正确;
B.反应有固体参加,达到平衡时,各物质的质量不变,则密度不变,故B正确;
C.T℃时,该反应的平衡常数K=$\frac{0.03×0.03}{(0.04)^{2}}$=$\frac{9}{16}$,故C错误;
D.正反应为吸热反应,升高温度,反应速率增大,且平衡正向移动,故D正确.
故选C.
点评 本题考查化学平衡计算与影响因素、化学平衡常数,为高频考点,侧重于学生的分析能力和计算能力的考查,难度中等,注意把握计算的思路以及C为固体的特点.

| A. | 纯碱(Na2CO3)从物质的分类看不属于碱 | |
| B. | 由一种元素组成的物质一定是单质 | |
| C. | 凡是能电离出H+的化合物均属于酸 | |
| D. | 盐类物质一定含有金属离子 |
 | 1.0 | 2.0 | 3.0 |
| 810 | 54.0 | a | b |
| 915 | c | 75.0 | d |
| 1000 | e | f | 83.0 |
④该反应△H<0;⑤K(1000℃)>K(810℃);
上述①~④中正确的有( )
| A. | 5个 | B. | 4个 | C. | 3个 | D. | 2个 |
| A. | A的平均反应速率为0.15mol/(L•min) | B. | B的转化率为20% | ||
| C. | B的平衡浓度为0.5mol/L | D. | x的数值为2 |
| A. | x值为1 | B. | 混合气体的密度增大 | ||
| C. | 平衡时N的浓度为 0.6 mol/L | D. | N的转化率为80% |
| A. | 用物质A表示的反应的平均速率为0.6mol•L-1•s-1 | |
| B. | 用物质B表示的反应的平均速率为0.6mol•L-1•s-1 | |
| C. | 2s时物质A的转化率为70% | |
| D. | 2s时物质B的物质的量为 1.4mol |
| 化学键 | H-H | C=O | C═O | C-H |
| E/(kJ•mol-1) | 436 | 803 | 1070 | 413 |
(2)CH4和CO2重整反应过程复杂,还会发生的反应有:
2CO(g)═C(s)+CO2(g)△H1=-172kJ/mol
CH4(g)═C(s)+2H2 (g)△H2
结合(1)中所给数据可得△H2=-74kJ/mol.
| A. | 用钢瓶储存液氯或浓硫酸 | |
| B. | 硅胶可用作食品干燥剂 | |
| C. | pM2.5是指大气中直径接近2.5×10-6m的颗粒物,它分散在空气中形成胶体 | |
| D. | 神舟10号飞船所用太阳能电池板的材料是单晶硅 |