题目内容
某小组为测定某碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数,甲、乙两组同学分别进行了下列相关实验.
方案Ⅰ.甲组同学用沉淀分析法,按如图所示的实验流程进行实验:[已知Ba(HCO3)2可溶于水]

(1)实验时,过滤操作中,除了玻璃棒、漏斗外,还要用到的玻璃仪器为 .
(2)洗涤沉淀B的操作是 .
(3)若实验中测得样品质量为m g,沉淀质量为n g,则碳酸钠的质量分数为 .
方案Ⅱ.乙组同学的主要实验流程图如下:
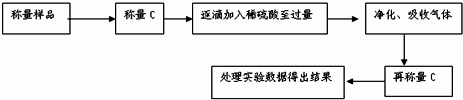
按如图1所示装置进行实验:

(4)该实验中装置B盛放的物质是 ,分液漏斗中 (填“能”或“不能”)用盐酸代替稀硫酸进行实验.
(5)在C中装碱石灰来吸收净化后的气体.
①样品中碳酸钠的质量分数越大,则实验中干燥管C在充分吸收气体前后的质量差 .(填“越大”、“越小”或“不变化”)
②D装置的作用是 .
(6)有同学认为为了减少实验误差,在反应前后都要通入N2(如图2),反应后通入N2的目的是 .
方案Ⅰ.甲组同学用沉淀分析法,按如图所示的实验流程进行实验:[已知Ba(HCO3)2可溶于水]

(1)实验时,过滤操作中,除了玻璃棒、漏斗外,还要用到的玻璃仪器为
(2)洗涤沉淀B的操作是
(3)若实验中测得样品质量为m g,沉淀质量为n g,则碳酸钠的质量分数为
方案Ⅱ.乙组同学的主要实验流程图如下:

按如图1所示装置进行实验:

(4)该实验中装置B盛放的物质是
(5)在C中装碱石灰来吸收净化后的气体.
①样品中碳酸钠的质量分数越大,则实验中干燥管C在充分吸收气体前后的质量差
②D装置的作用是
(6)有同学认为为了减少实验误差,在反应前后都要通入N2(如图2),反应后通入N2的目的是
考点:探究物质的组成或测量物质的含量,钠的重要化合物
专题:实验探究和数据处理题
分析:方案Ⅰ、样品溶液后加入氯化钡,碳酸钠和氯化钡反应生成碳酸钡沉淀,碳酸氢钠与氯化钡不反应,过滤、干燥得到碳酸钡沉淀,通过碳酸钡沉淀可求出碳酸钠的物质的量,进而求得碳酸钠的质量分数.
(1)根据过滤操作分析所需仪器;
(2)根据洗涤沉淀的操作回答;
(3)沉淀n为碳酸钡,根据碳守恒,碳酸钠的物质的量和碳酸钡相等,进而计算质量分数;
方案Ⅱ、碳酸钠和碳酸氢钠与稀硫酸反应生成二氧化碳,把除去水蒸气的二氧化碳被碱石灰吸收,通过碱石灰的增重求得二氧化碳的质量,根据二氧化碳的质量和样品质量求得碳酸钠的物质的量,进而求得质量分数.
(4)装置B的作用是把气体中的水蒸气除去;分液漏斗中如果用盐酸代替硫酸,盐酸易挥发;
(5)①等质量碳酸钠和碳酸氢钠与硫酸反应,碳酸氢钠产生二氧化碳多;
②空气中的水蒸气和二氧化碳会被碱石灰吸收;
(6)该方案关键是要获得产生的CO2的质量,故应保证产生的二氧化碳完全被吸收,而空气中二氧化碳不能被吸收.
(1)根据过滤操作分析所需仪器;
(2)根据洗涤沉淀的操作回答;
(3)沉淀n为碳酸钡,根据碳守恒,碳酸钠的物质的量和碳酸钡相等,进而计算质量分数;
方案Ⅱ、碳酸钠和碳酸氢钠与稀硫酸反应生成二氧化碳,把除去水蒸气的二氧化碳被碱石灰吸收,通过碱石灰的增重求得二氧化碳的质量,根据二氧化碳的质量和样品质量求得碳酸钠的物质的量,进而求得质量分数.
(4)装置B的作用是把气体中的水蒸气除去;分液漏斗中如果用盐酸代替硫酸,盐酸易挥发;
(5)①等质量碳酸钠和碳酸氢钠与硫酸反应,碳酸氢钠产生二氧化碳多;
②空气中的水蒸气和二氧化碳会被碱石灰吸收;
(6)该方案关键是要获得产生的CO2的质量,故应保证产生的二氧化碳完全被吸收,而空气中二氧化碳不能被吸收.
解答:
解:(1)用漏斗制作过滤器,过滤时用玻璃棒引流,用烧杯盛滤液,故答案为:烧杯;
(2)洗涤沉淀的操作是在过滤器中加水浸没沉淀使水自然留下,重复操作2-3次,
故答案为:用玻璃棒引流,注入蒸馏水,直至刚好没过沉淀,待水从漏斗底部自然流完后,重复上述操作2-3次;
(3)沉淀n为碳酸钡,物质的量
=
mol,根据碳守恒,碳酸钠的物质的量和碳酸钡相等,故碳酸钠的物质的量为:
mol,碳酸钠的质量分数为:
×100%=
×100%,故答案为:
×100%;
Ⅱ、(4)装置B的作用是把气体中的水蒸气除去,故用浓硫酸来除去水蒸气;分液漏斗中如果用盐酸代替硫酸,盐酸易挥发,这样制得二氧化碳气体中含氯化氢,浓硫酸不能吸收氯化氢,则氯化氢被碱石灰吸收,导致测到二氧化碳质量偏高,等质量碳酸钠和碳酸氢钠,碳酸氢钠产生二氧化碳多,则会导致碳酸氢钠偏多,碳酸钠偏小;故答案为:浓硫酸;不能;
(5)①等质量碳酸钠和碳酸氢钠,碳酸氢钠产生二氧化碳多,故若样品中碳酸钠的质量分数越大,则产生二氧化碳越少,则实验中干燥管C在充分吸收气体前后的质量差就越小;故答案为:越小;
②空气中的水蒸气和二氧化碳会被碱石灰吸收,故D的作用是吸收空气中的水蒸气和二氧化碳,以确保C装置中质量增加量的准确性;
故答案为:吸收空气中的水蒸气和二氧化碳,以确保C装置中质量增加量的准确性;
(6)该方案关键是要获得产生的CO2的质量,实验前容器内含有空气,空气中含有二氧化碳,会影响生成的二氧化碳的量,反应后装置中容器内含有二氧化碳,不能被C中碱石灰完全吸收,导致测定结果有较大误差,所以反应前后都要通入N2,反应后通入N2的目的是:排尽装置内的空气,将生成的二氧化碳从容器内排出,被C装置中碱石灰吸收,故答案为:排尽装置内的空气,将生成的二氧化碳从容器内排出,被C装置中碱石灰吸收.
(2)洗涤沉淀的操作是在过滤器中加水浸没沉淀使水自然留下,重复操作2-3次,
故答案为:用玻璃棒引流,注入蒸馏水,直至刚好没过沉淀,待水从漏斗底部自然流完后,重复上述操作2-3次;
(3)沉淀n为碳酸钡,物质的量
| ng |
| 197g/mol |
| n |
| 197 |
| n |
| 197 |
| ||
| mg |
| 106n |
| 197m |
| 106n |
| 197m |
Ⅱ、(4)装置B的作用是把气体中的水蒸气除去,故用浓硫酸来除去水蒸气;分液漏斗中如果用盐酸代替硫酸,盐酸易挥发,这样制得二氧化碳气体中含氯化氢,浓硫酸不能吸收氯化氢,则氯化氢被碱石灰吸收,导致测到二氧化碳质量偏高,等质量碳酸钠和碳酸氢钠,碳酸氢钠产生二氧化碳多,则会导致碳酸氢钠偏多,碳酸钠偏小;故答案为:浓硫酸;不能;
(5)①等质量碳酸钠和碳酸氢钠,碳酸氢钠产生二氧化碳多,故若样品中碳酸钠的质量分数越大,则产生二氧化碳越少,则实验中干燥管C在充分吸收气体前后的质量差就越小;故答案为:越小;
②空气中的水蒸气和二氧化碳会被碱石灰吸收,故D的作用是吸收空气中的水蒸气和二氧化碳,以确保C装置中质量增加量的准确性;
故答案为:吸收空气中的水蒸气和二氧化碳,以确保C装置中质量增加量的准确性;
(6)该方案关键是要获得产生的CO2的质量,实验前容器内含有空气,空气中含有二氧化碳,会影响生成的二氧化碳的量,反应后装置中容器内含有二氧化碳,不能被C中碱石灰完全吸收,导致测定结果有较大误差,所以反应前后都要通入N2,反应后通入N2的目的是:排尽装置内的空气,将生成的二氧化碳从容器内排出,被C装置中碱石灰吸收,故答案为:排尽装置内的空气,将生成的二氧化碳从容器内排出,被C装置中碱石灰吸收.
点评:本题考查了物质性质的探究和组成分析判断,主要是实验过程的分析,掌握基本操作和测定原理是解题关键,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
某物质可能有甲酸、乙酸、甲醇和甲酸乙酯四种物质中的一种或几种,在鉴定时有下列现象:下列叙述正确的是( )
①有银镜反应,
②加入新制Cu(OH)2悬浊液沉淀不溶解,
③与含酚酞的NaOH溶液共热,发现溶液中红色逐渐褪去以至无色.
①有银镜反应,
②加入新制Cu(OH)2悬浊液沉淀不溶解,
③与含酚酞的NaOH溶液共热,发现溶液中红色逐渐褪去以至无色.
| A、几种物质都有 |
| B、有甲酸乙酯和甲酸 |
| C、有甲酸乙酯和甲醇 |
| D、有甲酸乙酯,可能有甲醇 |
乙烯制聚乙烯,所发生的反应属于( )
| A、加成反应 | B、加聚反应 |
| C、取代反应 | D、酯化反应 |
 三氯化铁是中学化学实验室中不可缺少的重要试剂.
三氯化铁是中学化学实验室中不可缺少的重要试剂.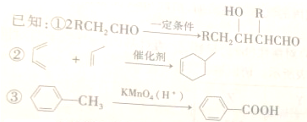
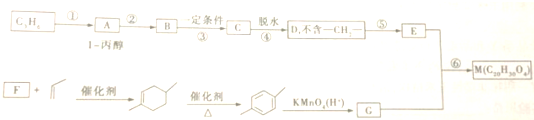

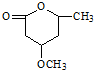 是B的一种重要的同分异构体.请设计合理方案,完成从
是B的一种重要的同分异构体.请设计合理方案,完成从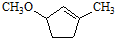 到
到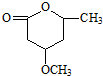 的合成路线(用合成路线流程图表示,并注明反应条件).
的合成路线(用合成路线流程图表示,并注明反应条件). …
…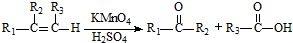 ;
;

