题目内容
钠原子与钠离子比较,相同的是( )
| A、核外电子层数 |
| B、最外层电子数 |
| C、能与水反应并放出H2 |
| D、焰色反应 |
考点:分子、原子、离子,钠的化学性质
专题:元素及其化合物
分析:A、钠原子具有3个电子层,失去最外层的1个电子后成为钠离子;
B、钠原子的最外层1个电子,钠离子最外层8个电子;
C、钠与水反应放出氢气,钠离子性质稳定不与水反应;
D、焰色反应是金属元素的性质.
B、钠原子的最外层1个电子,钠离子最外层8个电子;
C、钠与水反应放出氢气,钠离子性质稳定不与水反应;
D、焰色反应是金属元素的性质.
解答:
解:A、钠原子具有3个电子层,失去最外层的1个电子后成为钠离子,钠离子有2个电子层,故A错误;
B、钠原子的最外层1个电子,钠离子最外层8个电子,故B错误;
C、钠与水反应放出氢气,钠离子性质稳定不与水反应,故C错误;
D、焰色反应是金属元素的性质.钠原子和钠离子的焰色反应均为黄色,故D正确.
故选:D.
B、钠原子的最外层1个电子,钠离子最外层8个电子,故B错误;
C、钠与水反应放出氢气,钠离子性质稳定不与水反应,故C错误;
D、焰色反应是金属元素的性质.钠原子和钠离子的焰色反应均为黄色,故D正确.
故选:D.
点评:本题考查了钠原子和钠离子的结构、性质的比较,难度不大,注意知识的积累.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
关于HOOC-CH═CH-CH2OH,下列说法不正确的是( )
| A、分子式为C4H6O3,每摩尔该物质充分燃烧需消耗4 mol O2 |
| B、能发生取代、加成、氧化、中和等反应 |
| C、分别与足量Na、NaOH、Na2CO3反应,生成物均为NaOOC-CH═CH-CH2OH |
| D、该物质分子内和分子间都能发生酯化反应 |
下列实验操作中所用仪器合理的是( )
| A、用25mL的碱式滴定管量取14.8mL NaOH溶液 |
| B、用100mL量筒量取5.2mL盐酸 |
| C、用托盘天平称取25.2g氯化钠 |
| D、用100mL容量瓶配制50mL 0.1mol/L盐酸 |
下列事实不能用勒夏特列原理来解释的是( )
| A、高压有利于氢气与氮气合成氨 |
| B、实验室中常用排饱和食盐水的方法收集Cl2 |
| C、用V2O5催化二氧化硫氧化为三氧化硫 |
| D、二氧化硫氧化为三氧化硫的过程中,增大氧气的浓度可以提高二氧化硫的转化率 |
脑白金是热卖中的一种滋补品,其有效成分的结构简式为 .下列对该化合物的叙述正确的是( )
.下列对该化合物的叙述正确的是( )
 .下列对该化合物的叙述正确的是( )
.下列对该化合物的叙述正确的是( )| A、它属于芳香烃 |
| B、它属于高分子化合物 |
| C、分子式为C13N2H17O2 |
| D、在一定条件下可以发生加成反应 |
下列说法不正确的是( )
| A、化学反应除了生成新物质外,还伴随着能量的变化 |
| B、物质燃烧和中和反应均放出热量 |
| C、化合反应肯定是吸热反应 |
| D、化学反应是吸热还是放热决定于生成物具有的总能量和反应物具有的总能量 |
有如下合成路线,甲经二步转化为丙:
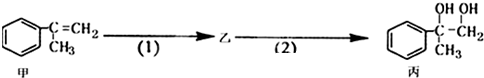
下列叙述错误的是( )
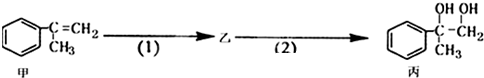
下列叙述错误的是( )
| A、物质丙能与浓硫酸加热发生消去反应 |
| B、甲和丙均可与酸性KMnO4溶液发生反应 |
| C、反应(1)需用铁作催化剂,反应(2)属于取代反应 |
| D、步骤(2)产物中可能含有未反应的甲,可用溴水检验是否含甲 |
 在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子.使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ?mol-1表示.请认真观察下图,然后回答问题.
在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子.使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ?mol-1表示.请认真观察下图,然后回答问题.