题目内容
目前关于上有一种方法是用CO和H2来生产甲醇,如图Ⅰ、图Ⅱ是关于该反应在一定条件下进行情况的图示.
请根据如图所示回答下列问题:
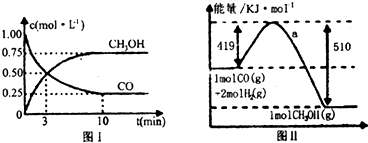
(1)如图Ⅰ是反应时CO和CH3OH的浓度随时间的变化情况,从反应开始至达到平衡时,用CO浓度变化表示的平均速率v(CO)=
(2)写出高反应的热化学方程式
(3)该反应的平衡常数K的表达式为 ;当温度升高时,该平衡常数K将 (填“增大”“减小”或“不变”)
(4)在恒温条件下,下列措施中能使
增大的有
A.升高温度B.充入氦气C.再充入1molCO和2molH2D.使用催化剂
(5)在恒温条件下,保持CO浓度不变,扩大容器体积,则平衡 (填“逆向移动”“正向移动”“不移动”)
请根据如图所示回答下列问题:

(1)如图Ⅰ是反应时CO和CH3OH的浓度随时间的变化情况,从反应开始至达到平衡时,用CO浓度变化表示的平均速率v(CO)=
(2)写出高反应的热化学方程式
(3)该反应的平衡常数K的表达式为
(4)在恒温条件下,下列措施中能使
| n(CH3OH) |
| n(CO) |
A.升高温度B.充入氦气C.再充入1molCO和2molH2D.使用催化剂
(5)在恒温条件下,保持CO浓度不变,扩大容器体积,则平衡
考点:化学平衡的影响因素,热化学方程式
专题:化学反应中的能量变化,化学平衡专题
分析:(1)根据图I时,反应中CO浓度的变化,结合速率公式计算;
(2)根据反应物与生成物的总能量来分析吸热还是放热,并书写热化学反应方程式;
(3)根据反应方程式结合平衡常数的含义书写;根据温度对平衡的影响分析K的变化;
(4)恒容条件下,下列措施中能使
增大,则平衡正移,据此分析;
(5)该反应是气体体积减小的反应,扩大容器体积,平衡向体积增大的方向移动,也就是平衡逆向移动,据此判断.
(2)根据反应物与生成物的总能量来分析吸热还是放热,并书写热化学反应方程式;
(3)根据反应方程式结合平衡常数的含义书写;根据温度对平衡的影响分析K的变化;
(4)恒容条件下,下列措施中能使
| n(CH3OH) |
| n(CO) |
(5)该反应是气体体积减小的反应,扩大容器体积,平衡向体积增大的方向移动,也就是平衡逆向移动,据此判断.
解答:
解:(1)由图I可知,反应中CO浓度的变化为1.00-0.25=0.75mol?L-1,则c(CO)=
=
=0.075mol/(L?min),故答案为:0.075mol/(L?min);
(2)反应物的总能量为419kJ,生成物的总能量为510kJ,则该反应为放热反应,放出的热量为419kJ-510kJ=91kJ,热化学方程式为CO(g)+2H2(g)=CH3OH(g)△H=-91 kJ/mol,故答案为:CO(g)+2H2(g)=CH3OH(g)△H=-91 kJ/mol;
(3)已知CO(g)+2H2(g)?CH3OH(g);则K=
;已知该反应的正方向为放热反应,升高温度平衡逆移,所以K减小,
故答案为:K=
;减小;
(4)恒容条件下,下列措施中能使
增大,则平衡正移;
A.已知该反应的正方向为放热反应,升高温度,平衡逆移,故A错误;
B.充入He气,容器的体积不变,各反应物的浓度不变,平衡不移动,故B错误;
C.再充入1molCO和2molH2,与原来加入了的量等比例,平衡时比原来的平衡的压强增大,平衡正移,故C正确;
D.使用催化剂,同等程度的改变正逆反应速率,平衡不移动,故D错误;
故答案为:C;
(5)该反应是气体体积减小的反应,扩大容器体积,平衡向体积增大的方向移动,也就是平衡逆向移动,故答案为:逆向移动.
| △c |
| t |
| 0.75mol?L |
| 10min |
(2)反应物的总能量为419kJ,生成物的总能量为510kJ,则该反应为放热反应,放出的热量为419kJ-510kJ=91kJ,热化学方程式为CO(g)+2H2(g)=CH3OH(g)△H=-91 kJ/mol,故答案为:CO(g)+2H2(g)=CH3OH(g)△H=-91 kJ/mol;
(3)已知CO(g)+2H2(g)?CH3OH(g);则K=
| c(CH3OH) |
| c(CO)?c2(H2) |
故答案为:K=
| c(CH3OH) |
| c(CO)?c2(H2) |
(4)恒容条件下,下列措施中能使
| n(CH3OH) |
| n(CO) |
A.已知该反应的正方向为放热反应,升高温度,平衡逆移,故A错误;
B.充入He气,容器的体积不变,各反应物的浓度不变,平衡不移动,故B错误;
C.再充入1molCO和2molH2,与原来加入了的量等比例,平衡时比原来的平衡的压强增大,平衡正移,故C正确;
D.使用催化剂,同等程度的改变正逆反应速率,平衡不移动,故D错误;
故答案为:C;
(5)该反应是气体体积减小的反应,扩大容器体积,平衡向体积增大的方向移动,也就是平衡逆向移动,故答案为:逆向移动.
点评:本题为综合性习题,考查影响化学平衡的因素、热化学反应、化学平衡常数、反应速率的计算,图象的分析和利用等知识点,注重对高考热点知识的考查,是较好的习题.

练习册系列答案
相关题目
如图是某有机物的球棍模型,下列关于该有机物的性质叙述中错误的是( )
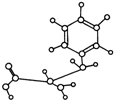

| A、能与NaOH发生反应,但不能与盐酸反应 |
| B、能合成高分子化合物 |
| C、能发生加成反应 |
| D、能发生水解反应 |
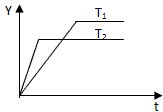 已知反应N2(g)+3H2(g)?2NH3(g);△H<0,向某压强恒定、体积可变的容器中按体积比1:3充入N2和H2,在一定条件下发生反应.如图是某物理量Y随时间(t)变化的示意图,Y可能是( )
已知反应N2(g)+3H2(g)?2NH3(g);△H<0,向某压强恒定、体积可变的容器中按体积比1:3充入N2和H2,在一定条件下发生反应.如图是某物理量Y随时间(t)变化的示意图,Y可能是( )| A、N2的转化率 |
| B、混合气体的平均摩尔质量 |
| C、容器的体积 |
| D、混合气体的密度 |
日本福岛核电站泄漏物中含有放射性的
I.有关
I的说法正确是( )
131 53 |
131 53 |
| A、核外电子数为78 | ||
B、与
| ||
| C、中子数为131 | ||
D、与
|
下列说法正确的是( )
| A、强电解质溶液的导电能力一定强于弱电解质溶液 |
| B、乙酸溶液中存在的微粒有CH3COOH、CH3COO-、H+、OH-、H2O |
| C、0.05mol的NaOH固体分别加入到体积都是100ml的自来水、0.5mol/L的乙酸、0.5mol/L的盐酸和0.5mol/L的NaCl溶液中,溶液导电能力变化最小的是自来水 |
| D、在相同温度下,a强电解质,b弱电解质,c金属Al的导电能力相同,升高温度后它们的导电能力都增强 |
已知4NH3+5O2?4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,正确的关系是( )
| A、4 v(NH3)=5v(O2) |
| B、6 v(O2)=5v(H2O) |
| C、4v(NH3)=6 v(H2O) |
| D、v(O2)=4v(NO) |
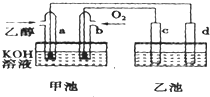 如图甲池和乙池中的四个电极都是惰性材料,溶液体积均为200mL,请根据图示回答下列问题
如图甲池和乙池中的四个电极都是惰性材料,溶液体积均为200mL,请根据图示回答下列问题