题目内容
14. 甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇(于固定容器中进行):2H2(g)+CO(g)?CH3OH(g)
甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇(于固定容器中进行):2H2(g)+CO(g)?CH3OH(g)(1)如表所列数据是该反应在不同温度下的化学平衡常数(K)
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
②要提高CO的转化率,可以采取的措施是df(填序号).
a.升温 b.加入催化剂 c.增加CO的浓度 d.加入H2加压
e.加入惰性气体加压 f.分离出甲醇
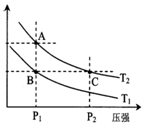
(2)如图表示在温度分别为T1、T2时,平衡体系中H2的体积分数随压强变化曲线,A、C两点的反应速率A<C(填“>”、“=”或“<”,下同),A、C两点的化学平衡常数A=C,由状态B到状态A,可采用升温的方法(填“升温”或“降温”).
分析 (1)①2H2(g)+CO(g)?CH3OH(g)反应气体的物质的量减少,依据化学方程式和平衡常数概念书写,依据平衡常数随温度变化判断反应能量变化;
②要提高CO的转化率,一般使平衡正向移动即可,但增加CO的浓度平衡虽然正向移动,但CO的转化率减小;
(2)根据压强越大反应速率越大判断;化学平衡常数仅与温度有关;由状态B到状态A,可采用升温的方法.
解答 解:(1)①2H2(g)+CO(g)?CH3OH(g)反应气体的物质的量减少,所以△S<0;由表中数据可知温度升高,K值减小,说明平衡向逆反应方向移动,逆反应为吸热反应,正反应即为放热反应△H<0,由△G=△H-T△S可知,反应在低温条件下能自发进行,故答案为:<;低温;
②a.升温平衡逆向移动,则CO的转化率减小,故错误;
b.加入催化剂平衡不移动,则CO的转化率不变,故错误;
c.增加CO的浓度,平衡虽然正向移动,但CO的转化率减小,故错误;
d.加入H2加压,平衡正向移动,CO的转化率提高,故正确;
e.加入惰性气体加压,平衡不移动,则CO的转化率不变,故错误;
f.分离出甲醇,平衡正向移动,CO的转化率提高,故正确;
故选:d f;
(2)因为压强越大反应速率越大,所以A、C两点的反应速率A<C;化学平衡常数仅与温度有关,所以A、C两点的化学平衡常数A=C;由状态B到状态A,可采用升温的方法,故答案为:<;=;升温.
点评 本题考查了平衡常数,平衡移动原理分析应等,掌握基础是关键,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.在密闭容器中的一定量混合气体发生反应:xA(g)+yB(g)?zC(g),平衡时测得A的浓度为0.60mol/L,保持温度不变,将容器的体积扩大两倍,测得A的浓度变为0.35mol/L,下列有关判断正确的是( )
| A. | x+y<z | B. | 平衡正向移动 | C. | A的转化率降低 | D. | C的物质的量增大 |
2.下列各组混合物中,能用分液漏斗进行分离的是( )
| A. | 水和CCl4 | B. | 液溴和CCl4 | C. | 酒精和水 | D. | 汽油和菜籽油 |
9.自来水可以用氯气消毒,下列哪些药品不能用氯气消毒的自来水配制的是( )
| A. | Na2SO4 | B. | NaCl | C. | AgNO3 | D. | AlCl3 |
6.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 1mol甲基中含有的电子数为10NA | |
| B. | 22g CO2中含有共用电子对数4NA个 | |
| C. | 标准状况下22.4L氯仿(三氯甲烷)中共价键数目为4NA | |
| D. | 28g C2H4中含有2NA个碳原子 |
3.在汽车加油站见到的油罐车上,所贴的危险化学品标志是( )
| A. |  | B. |  | C. |  | D. |  |
4.下列有机物的命名正确的是( )
| A. | 2-甲基-3-丁烯 | B. | 1-甲基乙醇 | C. | 2-乙基丙烷 | D. | 乙基苯 |