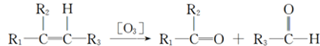题目内容
下列有关沉淀溶解平衡的说法中,正确的是( )
| A、在AgCl的沉淀溶解平衡体系中,加入蒸馏水,Ksp(AgCl)增大 |
| B、可直接根据Ksp的数值大小比较难溶物在水中的溶解度大小 |
| C、在CaCO3的沉淀溶解平衡体系中,加入稀盐酸,平衡不移动 |
| D、25℃时,Ksp(AgCl)>Ksp(AgI),向AgCl的悬浊液中加入KI溶液,有黄色沉淀生成 |
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:A.难溶盐电解质的Ksp与温度有关,不受其他因素的影响;
B.比较不同类型的难溶物的溶解度大小,必须通过计算溶解度比较,不能通过溶度积直接比较,比较同类型的难溶物的溶解度大小,可通过溶度积直接比较溶解度大小;
C.加入稀盐酸,与碳酸根离子反应,溶液中CO32-浓度减小,根据平衡移动原理,平衡向CO32-浓度减小的方向移动;
D.沉淀转化为溶解度更小的物质容易发生.
B.比较不同类型的难溶物的溶解度大小,必须通过计算溶解度比较,不能通过溶度积直接比较,比较同类型的难溶物的溶解度大小,可通过溶度积直接比较溶解度大小;
C.加入稀盐酸,与碳酸根离子反应,溶液中CO32-浓度减小,根据平衡移动原理,平衡向CO32-浓度减小的方向移动;
D.沉淀转化为溶解度更小的物质容易发生.
解答:
解:A.因难溶盐电解质的Ksp与温度有关,不受其他因素的影响,所以加入蒸馏水,氯化银的KSP不变,故A错误;
B.比较不同类型的难溶物的溶解度大小,必须通过计算溶解度比较,不能通过溶度积直接比较,故B错误;
C.碳酸根离子与酸反应生成二氧化碳和水,生成物的浓度减小,碳酸钙的沉淀溶解平衡正向移动,故C错误;
D.KSP(AgCl)>KSP(AgI),沉淀转化为溶解度更小的物质容易发生,向AgCl的悬浊液中加入KI溶液,沉淀由白色转化为黄色,故D正确;
故选:D.
B.比较不同类型的难溶物的溶解度大小,必须通过计算溶解度比较,不能通过溶度积直接比较,故B错误;
C.碳酸根离子与酸反应生成二氧化碳和水,生成物的浓度减小,碳酸钙的沉淀溶解平衡正向移动,故C错误;
D.KSP(AgCl)>KSP(AgI),沉淀转化为溶解度更小的物质容易发生,向AgCl的悬浊液中加入KI溶液,沉淀由白色转化为黄色,故D正确;
故选:D.
点评:本题考查难溶电解质的溶解平衡及沉淀转化的本质,注意沉淀转化为溶解度更小的物质容易发生.

练习册系列答案
相关题目
下列物质是有机化合物的是( )
| A、CO2 |
| B、NaCl |
| C、乙醇(CH3CH2OH) |
| D、CaCO3 |
将一定量的固体Ag2SO4置于容积不变的容器中(装有少量V2O5),在某温度下发生反应:Ag2SO4(s)?Ag2O(s)+SO3(g),2SO3(g)?2SO2(g)+O2(g).反应经过10min达到平衡,测得c(SO3)=0.4mol/L、c(SO2)=0.1mol/L,则下列叙述中不正确的是( )
| A、容器里气体的密度为40 g/L |
| B、SO3的分解率为20% |
| C、在这10 min内的平均速率为υ(O2)=0.005 mol?L-1?min-1 |
| D、化学反应速率:υ(Ag2SO4)=υ(SO3) |
在5L密闭容器中,1molA和3molB在一定条件下反应:A(g)+mB(g)?2C(g),经3min反应达到平衡状态,测得混合气体共3.2mol,其中含0.8molC,则下列说法不正确的是( )
| A、m值等于3 |
| B、平衡时,体系中c(A):c(B):c(C)=4:9:8 |
| C、A的转化率为40% |
| D、用B表示该反应的平均反应速率为0.08mol?L-1?min-1 |

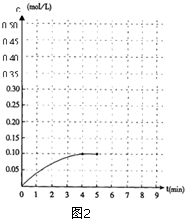 内加入0.2mol的N2和0.6mol 的H2,在一定条件下发生如下反应:N2 (g)+3H2(g)?2NH3(g)△H<0.反应中NH3的物质的量浓度的变化的情况如图2:
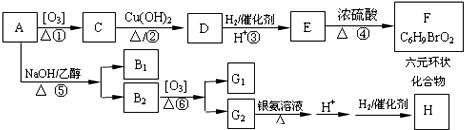
内加入0.2mol的N2和0.6mol 的H2,在一定条件下发生如下反应:N2 (g)+3H2(g)?2NH3(g)△H<0.反应中NH3的物质的量浓度的变化的情况如图2: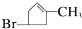 .化合物A~H的转化关系如图所示,B1和B2互为同分异构体,B1的摩尔质量80g/mol;G1和G2互为同分异构体,核磁共振氢谱显示二者均只有两种氢,G1无甲基.请完成下列问题.
.化合物A~H的转化关系如图所示,B1和B2互为同分异构体,B1的摩尔质量80g/mol;G1和G2互为同分异构体,核磁共振氢谱显示二者均只有两种氢,G1无甲基.请完成下列问题.