题目内容
8.下列各组物质的稀溶液相互反应,无论是前者滴入后者,还是后者滴入前者,反应现象都相同的是( )| A. | NaAlO2 和 HCl | B. | MgCl2和 NH3•H2O | C. | Na2CO3和HCl | D. | AlCl3和NaOH |
分析 各组溶液无论是前者滴入后者,还是把后者滴入前者,所得现象相同,说明该混合溶液中发生的反应与反应物的量无关,据此分析解答.
解答 解:A.偏铝酸钠和少量盐酸反应生成氢氧化铝沉淀,和过量盐酸反应生成氯化铝,所以反应现象不同,故A不选;
B.无论氨水是否过量,氯化镁和氨水反应都生成氢氧化镁沉淀,所以反应现象相同,故B正确;
C.碳酸钠滴入盐酸发生反应:Na2CO3+2HCl═2NaCl+CO2↑+H2O,现象立刻产生气泡;盐酸滴入碳酸钠发生反应:Na2CO3+HCl═NaHCO3+NaCl、NaHCO3+HCl═NaCl+CO2↑+H2O,现象开始无气泡,一段时间后有气泡,所以二者现象不同,故C不选;
D.当AlCl3少量时,氯化铝和氢氧化钠溶液反应生成偏铝酸钠,当AlCl3过量时,二者反应生成氢氧化铝沉淀,所以反应现象不同,故不选;
故选B.
点评 本题考查了物质的之间的反应,明确物质的性质及反应物用量对反应的影响是解题关键,题目难度不大.

练习册系列答案
相关题目
20.下列有关说法正确的是( )
| A. | 能在水溶液电离出H+的物质是酸 | |
| B. | 氧化还原反应中所有元素的化合价均有升降 | |
| C. | 在化学反应中,得电子越多的氧化剂,其氧化性就越强 | |
| D. | 氧化还原反应的实质是电子的转移(得失或偏移) |
3.我国科学家屠呦呦因发现青蒿素(化学式是C15H22O5),而获得2015年诺贝尔奖.青蒿素属于( )
| A. | 碱 | B. | 盐 | C. | 氧化物 | D. | 有机物 |
13.有关物质结构的下列说法中正确的是( )
| A. | 碘升华时破坏了共价键 | |
| B. | PH3沸点低于NH3沸点,因为P-H键键能低 | |
| C. | HF的分子间作用力(含有氢键)大于HCl,故HF比HCl更稳定 | |
| D. | 氯化钠固体中的离子键在溶于水时被破坏 |
20.化学科学需要借助化学语言来描述,下列化学用语正确的是( )
| A. | 甲烷分子的球棍模型: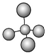 | B. | NH4Br的电子式: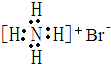 | ||
| C. | 34S2-的结构示意图: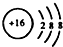 | D. | 邻羟基甲苯酸的结构简式: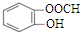 |
17.某化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图Ⅰ~Ⅳ所示.下列有关评价正确的是( )
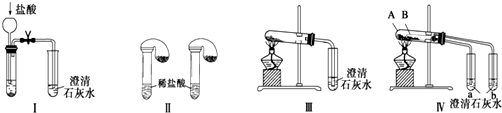

| A. | 根据图Ⅰ所示实验,可以根据澄清石灰水是否变浑浊鉴别碳酸钠和碳酸氢钠固体 | |
| B. | 在图Ⅱ所示实验的左右两只试管中加入足量的盐酸,然后向两个气球中分别加入等物质的量的碳酸钠和碳酸氢钠固体,根据反应后气球的大小可鉴别两种固体 | |
| C. | 与实验Ⅲ相比,实验Ⅳ的突出优点是可以做到用一套装置同时进行两个对比实验,而Ⅲ不行 | |
| D. | 若用实验Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则小试管B中装入的固体是碳酸钠 |
18.下列有关钠、铁、铝性质的说法中不正确的是( )
| A. | 在地壳中的含量:Al>Fe>Na | |
| B. | 均能与盐酸反应,但金属钠与盐酸的反应最剧烈 | |
| C. | 钠、铝均能从FeCl3溶液中置换出铁单质 | |
| D. | 钠、铝均能与NaOH溶液反应,但参加反应的物质种类前者少于后者 |

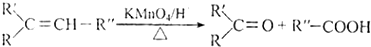
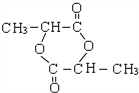
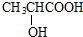 +HBr$\stackrel{△}{→}$CH3CHBrCOOH+H2O
+HBr$\stackrel{△}{→}$CH3CHBrCOOH+H2O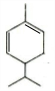 ,A与等物质的量的Br2进行加成反应的产物共有3种.(不考虑立体异构)
,A与等物质的量的Br2进行加成反应的产物共有3种.(不考虑立体异构)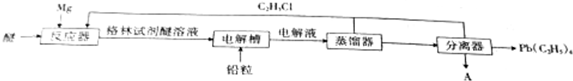
 ,电解物质A的化学方程式为MgCl2$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑.
,电解物质A的化学方程式为MgCl2$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑.