题目内容
4.从樟科植物枝叶提取的精油中含有一种有机物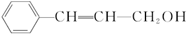 ,则对该有机物的说法正确的是( )
,则对该有机物的说法正确的是( )| A. | 能使溴水、酸性高锰酸钾溶液褪色 | |
| B. | 分子中所有原子在同一平面内 | |
| C. | 分子式为C9H12O | |
| D. | 能发生加成反应、酯化反应、水解反应 |
分析 有机物中含有碳碳双键,可发生加成、加聚和氧化反应,含有羟基,可发生取代、消去和氧化反应,以此解答该题.
解答 解:A.分子中含有碳碳双键,可发生加成反应,使溴水褪色,也可被酸性高锰酸钾氧化,故A正确;
B.分子中含有饱和碳原子,并不是所用的原子都在同一个平面上,故B错误;
C.由结构简式可知分子式为C9H10O,故C错误;
D.含有碳碳双键,羟基,可发生加成、酯化反应,但不能发生水解反应,故D错误.
故选A.
点评 本题考查有机物的结构与性质,为高考常见题型,侧重考查学生的分析能力,注意把握官能团和性质的关系,熟悉醇、烯烃的性质即可解答,题目难度不大.

练习册系列答案
相关题目
15.下列说法不正确的是( )
| A. | 有机物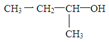 的名称为2-丁醇 的名称为2-丁醇 | |
| B. | 蛋白质、淀粉、纤维素都是高分子化合物 | |
| C. | 合成有机物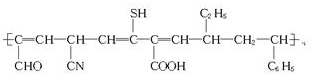 使用的单体有3种 使用的单体有3种 | |
| D. | 等质量的乙烯和乙醇完全燃烧消耗氧气的量相同 |
12.已知X、Y是主族元素,I为电离能,单位是kJ•mol-1.请根据下表所列数据判断,错误的是( )
| 元素 | I1 | I2 | I3 | I4 |
| X | 500 | 4600 | 6900 | 9500 |
| Y | 780 | 1300 | 2100 | 11600 |
| A. | 若元素Y处于第三周期,它可与冷水剧烈反应 | |
| B. | 元素X的常见化合价是+1 | |
| C. | 元素Y是ⅢA族元素 | |
| D. | 元素X与氯形成化合物时,化学式可能是XCl |
19.乙苯的二氯代物共有( )
| A. | 6种 | B. | 9种 | C. | 12种 | D. | 15种 |
9.已知反应A2(g)+2B2(g)?2AB2(g)△H<0,下列说法正确的是( )
| A. | 达平衡后降低温度,混合气体平均相对分子质量减小 | |
| B. | 使用催化剂能加快反应速率,缩短达平衡所需的时间且提高A2的转化率 | |
| C. | 达平衡后升高温度并增大压强,有可能每一组分的百分含量都不改变,但平衡常数一定发生改变 | |
| D. | 达平衡后,降低温度或减小压强都有利于该平衡向正反应方向移动 |
16.有8种物质:①乙烷;②乙烯;③乙炔;④苯;⑤甲苯;⑥溴乙烷;⑦聚丙烯;⑧聚乙炔.其中既能使酸性KMnO4溶液褪色,也能与溴水反应而使溴水褪色的是( )
| A. | ②③⑤ | B. | ②③⑦ | C. | ②③⑧ | D. | ②③⑦⑧ |
13.下列实验现象与结论不一致的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 等体积等浓度的HA和HB两种酸分别与足量的锌反应,用排水法收集气体 | HA放出氢气的反应速率更快 | 酸性:HB<HA |
| B | 以铜、铁、浓硝酸构成原电池 | 铁表面有红棕色气泡产生 | 铜作原电池的负极 |
| C | 向25mL冷水和沸水中分别滴入5滴FeCls饱和溶液 | 前者为黄色,后者为红褐色 | 升高温度,Fe3+的水解程度增大 |
| D | 将固体CaSO4加入Na2CO3饱和溶液中 | 一段时间后,检验固体主要成分为CaCO3 | Ksp ( CaSO4)<Ksp ( CaCO3 ) |
| A. | A | B. | B | C. | C | D. | D |
 .
.