题目内容
下列说法中,不符合VⅡA族元素性质特征的是( )
| A、易形成一价离子 |
| B、从上到下单质的氧化性逐渐减弱 |
| C、从上到下氢化物的沸点逐渐升高 |
| D、从上到下氢化物的稳定逐渐减弱 |
考点:同一主族内元素性质递变规律与原子结构的关系
专题:
分析:A、ⅦA族元素非金属性较强,易得一个电子形成8电子稳定结构;
B、ⅦA族元素从上到下得电子能力减弱;
C、相对分子质量越大,氢化物的沸点越高,含有氢键的沸点较高;
D、元素的非金属越弱,对应的氢化物的稳定性越弱.
B、ⅦA族元素从上到下得电子能力减弱;
C、相对分子质量越大,氢化物的沸点越高,含有氢键的沸点较高;
D、元素的非金属越弱,对应的氢化物的稳定性越弱.
解答:
解:A、ⅦA族元素非金属性较强易得一个电子形成8电子稳定结构,即易形成-1价离子,故A正确;
B、ⅦA族元素从上到下电子层在增多,得电子能力减弱,单质的氧化性逐渐减弱,故B正确;
C、相对分子质量越大,氢化物的沸点越高,含有氢键的沸点较高,所以氢化物的沸点HF>HI>HBr>HCl,故C错误;
D、元素的非金属越弱,对应的氢化物的稳定性越弱,ⅦA族元素从上到下非金属性减弱,则对应的氢化物的稳定性依次减弱,故D正确;
故选C.
B、ⅦA族元素从上到下电子层在增多,得电子能力减弱,单质的氧化性逐渐减弱,故B正确;
C、相对分子质量越大,氢化物的沸点越高,含有氢键的沸点较高,所以氢化物的沸点HF>HI>HBr>HCl,故C错误;
D、元素的非金属越弱,对应的氢化物的稳定性越弱,ⅦA族元素从上到下非金属性减弱,则对应的氢化物的稳定性依次减弱,故D正确;
故选C.
点评:本题考查ⅦA族元素性质,熟悉原子结构及元素周期表、元素周期律即可解答,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列各组离子能大量共存,且溶液为无色透明的是( )
| A、Al3+、AlO2-、NO3-、Cl- |
| B、CrO42-、H+、K+、NO3- |
| C、Ba2+、Na+、HCO3-、OH- |
| D、K+、SO42-、S2-、Na+ |
下列分类标准不正确的是( )
| A、化学反应分为:离子反应、非离子反应(标准:是否在水溶液中进行) |
| B、分散系分为:溶液、胶体、浊液(标准:分散质粒子的大小) |
| C、化学反应分为:氧化还原反应、非氧化还原反应(标准:元素化合价是否发生变化) |
| D、化合物分为:电解质、非电解质(标准:溶于水或熔融状态能否导电) |
下列离子在溶液中能大量共存,且通入过量SO2后无沉淀生成的一组是( )
| A、K+、Ba2+、Cl-、NO3- |
| B、K+、Na+、Br-、S2- |
| C、H+、Fe3+、I-、NO3- |
| D、Na+、Ba2+、OH-、Cl- |

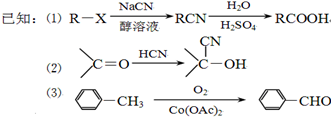
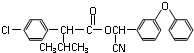 ):
):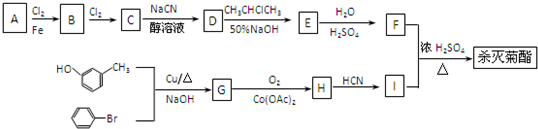
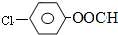 结构,则符合此条件的F共有
结构,则符合此条件的F共有