题目内容
2.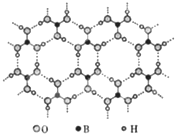 正硼酸(H3BO3)是一种层状结构白色晶体,层内的H3BO3分子通过氢键相连(如图).下列有关说法错误的是( )
正硼酸(H3BO3)是一种层状结构白色晶体,层内的H3BO3分子通过氢键相连(如图).下列有关说法错误的是( )| A. | 正硼酸晶体属于分子晶体 | B. | H3BO3分子的稳定性与氢键有关 | ||
| C. | 分子中硼原子最外层不是8e-结构 | D. | 含1mol H3BO3的晶体中有3mol氢键 |
分析 A.根据晶体中存在的微粒确定晶体类型;
B.分子的稳定性与化学键有关;
C.硼原子最外层只有3个电子,与氧原子形成3对共用电子对;
D.利用均摊法计算含1molH3BO3的晶体中的氢键.
解答 解:A.正硼酸晶体中存在H3BO3分子,且该晶体中存在氢键,说明硼酸由分子构成,是分子晶体,故A正确;
B.分子的稳定性与分子内的B-O、H-O共价键有关,熔沸点与氢键有关,故B错误.
C.硼原子最外层只有3个电子,与氧原子形成3对共用电子对,因此B原子不是8e-稳定结构,故C正确;
D.1个硼酸分子形成了6个氢键,但每个氢键是2个硼酸分子共用的,所以平均含3个氢键,则含有1molH3BO3的晶体中有3mol氢键,故D正确;
故选B.
点评 本题考查了晶体类型的判断、影响分子稳定性的因素、氢键的计算等知识点,难度不大,注意分子的稳定性与化学键有关,物质的熔沸点与氢键有关.

练习册系列答案
相关题目
3.下列物质中主要成分为纤维素的是( )
| A. | 尼龙 | B. | 黏胶纤维 | C. | 硝化纤维 | D. | 醋酸纤维 |
4.钴的氧化物广泛应用于磁性材料及超导材料等领域.取0.2mol Co5O6(其中结合钴的化合价为+2、+3),用足量浓盐酸溶解,得到CoCl2溶液和4.48L(标准状况)黄绿色气体,则原化合物中+2价Co的物质的量为( )
| A. | 0.2mol | B. | 0.4mol | C. | 0.6mol | D. | 0.8mol |
17.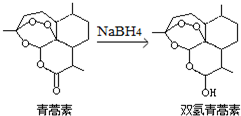 我国科学家屠呦呦获得2015年诺贝尔生理学或医学奖.她研究的青蒿素、双氢青蒿素在寄生虫疾病治疗方面取得了伟大成就.下列有关说法正确的是( )
我国科学家屠呦呦获得2015年诺贝尔生理学或医学奖.她研究的青蒿素、双氢青蒿素在寄生虫疾病治疗方面取得了伟大成就.下列有关说法正确的是( )
 我国科学家屠呦呦获得2015年诺贝尔生理学或医学奖.她研究的青蒿素、双氢青蒿素在寄生虫疾病治疗方面取得了伟大成就.下列有关说法正确的是( )
我国科学家屠呦呦获得2015年诺贝尔生理学或医学奖.她研究的青蒿素、双氢青蒿素在寄生虫疾病治疗方面取得了伟大成就.下列有关说法正确的是( )| A. | 青蒿素易溶于水 | |
| B. | 青蒿素可与NaOH溶液反应 | |
| C. | 青蒿素转化为双氢青蒿素是氧化反应 | |
| D. | 青蒿素有11种一氯代物 |
11.化学反应中会出现“一种物质过量,另一种物质仍不能完全反应”的特殊情况.下列反应中属于这种情况的是( )
①过量稀硫酸与块状石灰石;
②过量的氢气与少量氮气在催化剂存在下充分反应;
③过量稀硝酸与银反应;
④过量铜与浓硫酸;
⑤浓盐酸与过量的MnO2
⑥过量的锌与18mol/L的硫酸反应.
①过量稀硫酸与块状石灰石;
②过量的氢气与少量氮气在催化剂存在下充分反应;
③过量稀硝酸与银反应;
④过量铜与浓硫酸;
⑤浓盐酸与过量的MnO2
⑥过量的锌与18mol/L的硫酸反应.
| A. | ③④⑥ | B. | ②③⑤ | C. | ①②④⑤ | D. | ①②③④⑤⑥ |
12.下列说法正确的是( )
| A. | 凡需要加热的反应一定是吸热反应 | |
| B. | 反应物的总能量不一定比生成物的总能量高 | |
| C. | 化学反应速率的大小主要取决于反应进行时的外界因素 | |
| D. | 催化剂都能加大化学反应速率,并提高原料的利用率和转化率 |
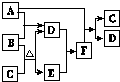 有A、B、C、D、E、F六种微粒,其中A~E五种微粒均由两种元素组成且均含10个电子,它们有如图所示的转化关系:
有A、B、C、D、E、F六种微粒,其中A~E五种微粒均由两种元素组成且均含10个电子,它们有如图所示的转化关系: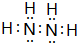 .
.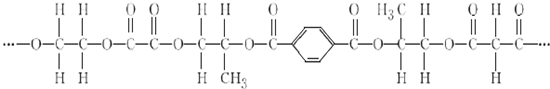
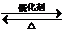
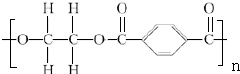 +2nH2O.
+2nH2O.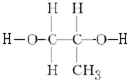 .
.
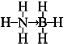 ;与氨硼烷互为等电子体的有机小分子是CH3CH3 (写结构简式).
;与氨硼烷互为等电子体的有机小分子是CH3CH3 (写结构简式).