题目内容
实验室用下列仪器、装置和药品制备并净化CO2,然后用CO2与Na2O2反应制取O2.
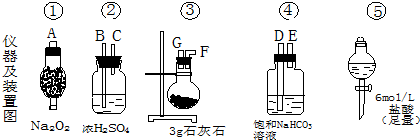
图中A、B、C、D、E、F、G表示玻璃管接口,接口的弯曲和伸长部分未画出.请根据要求填写下列空白.
(1)装置②的作用是 .
(2)若所制取的气体按从左向右流向时,上述各仪器、装置的组装顺序是(填各仪器、装置的序号) 接③接 接 接 .其中②与④装置相连时,玻璃管接口应是 接 .(填接口的字母)
(3)装置④中发生反应的离子方程式是 .
(4)请用集气瓶、量筒、导管、双孔塞,设计一个测定O2体积的装置,在方框中画出你设计的装置图 .
(5)已知:所用石灰石的实际纯度(CaCO3的质量分数)为60%,且其中杂质不与盐酸反应.为使实验顺利进行,需Na2O2过量,则Na2O2的质量范围是 g;某同学在上述实验中测得产生的O2共224mL(标准状况下测定,不考虑损失),则该同学测出的石灰石的纯度(CaCO3的质量分数)为 ,石灰石的测定纯度与实际纯度之间产生误差的原因是 .

图中A、B、C、D、E、F、G表示玻璃管接口,接口的弯曲和伸长部分未画出.请根据要求填写下列空白.
(1)装置②的作用是
(2)若所制取的气体按从左向右流向时,上述各仪器、装置的组装顺序是(填各仪器、装置的序号)
(3)装置④中发生反应的离子方程式是
(4)请用集气瓶、量筒、导管、双孔塞,设计一个测定O2体积的装置,在方框中画出你设计的装置图
(5)已知:所用石灰石的实际纯度(CaCO3的质量分数)为60%,且其中杂质不与盐酸反应.为使实验顺利进行,需Na2O2过量,则Na2O2的质量范围是
考点:制备实验方案的设计
专题:实验题
分析:实验目的是制备并净化CO2,然后用CO2与Na2O2反应制取O2,则由题给物质可知,应用盐酸和石灰石反应生成二氧化碳,用饱和碳酸氢钠除去二氧化碳气体中混有的HCl气体,然后应浓硫酸干燥二氧化碳,得到纯净的二氧化碳再和过氧化钠反应,以此确定装置的连接顺序,结合题目要求和物质的性质解答该题.
解答:
解:(1)盐酸和石灰石反应生成的二氧化碳中混有水蒸气,为得到干燥、纯净的二氧化碳气体,应用浓硫酸进行干燥,故答案为:干燥CO2气体;
(2)盐酸和石灰石反应生成二氧化碳,用饱和碳酸氢钠除去二氧化碳气体中混有的HCl气体,然后应浓硫酸干燥二氧化碳,得到纯净的二氧化碳再和过氧化钠反应,则连接的顺序为⑤→③→④→②→①,其中②与④装置相连时,玻璃管接口应是E连接B,注意洗气时气体应长进短出,
故答案为:⑤;④;②;①;E;B;
(3)④用于除去HCl,反应的离子方程式为H++HCO3-=H2O+CO2↑,故答案为:H++HCO3-=H2O+CO2↑;
(4)用集气瓶、量筒、导管、双孔塞,设计一个测定O2体积的装置,可将气体把集气瓶中的水排入到量筒中测量体积,装置图为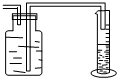 ,
,
故答案为: ;
;
(5)m(CaCO3)=3g×60%=1.8g,则与盐酸反应生成的二氧化碳物质的量为n(CO2)=n(CaCO3)=
=0.018mol,
与过氧化钠反应的方程式为2Na2O2+2CO2=2Na2CO3+O2,由方程式可知n(Na2O2)=0.018mol,则质量应大于0.018mol×78g/mol=1.404g,
如n(O2)=
=0.01mol,方程式为2Na2O2+2CO2=2Na2CO3+O2,则由方程式可知需要n(Na2O2)=0.02mol,则需要n(CO2)=0.02mol,
所以m(CaCO3)=0.02mol×100g/mol=2g,
则该同学测出的石灰石的纯度(CaCO3的质量分数)为
×100%=66.67%,
测得的质量分数偏大,可能原因是在除HCl时,NaHCO3与HCl反应生成了少量的CO2,使CO2的总体积增多,从而使石灰石的测定纯度偏大,
故答案为:>1.404;66.67%;在除HCl时,NaHCO3与HCl反应生成了少量的CO2,使CO2的总体积增多,从而使石灰石的测定纯度偏大.
(2)盐酸和石灰石反应生成二氧化碳,用饱和碳酸氢钠除去二氧化碳气体中混有的HCl气体,然后应浓硫酸干燥二氧化碳,得到纯净的二氧化碳再和过氧化钠反应,则连接的顺序为⑤→③→④→②→①,其中②与④装置相连时,玻璃管接口应是E连接B,注意洗气时气体应长进短出,
故答案为:⑤;④;②;①;E;B;
(3)④用于除去HCl,反应的离子方程式为H++HCO3-=H2O+CO2↑,故答案为:H++HCO3-=H2O+CO2↑;
(4)用集气瓶、量筒、导管、双孔塞,设计一个测定O2体积的装置,可将气体把集气瓶中的水排入到量筒中测量体积,装置图为
 ,
,故答案为:
 ;
;(5)m(CaCO3)=3g×60%=1.8g,则与盐酸反应生成的二氧化碳物质的量为n(CO2)=n(CaCO3)=
| 1.8g |
| 100g/mol |
与过氧化钠反应的方程式为2Na2O2+2CO2=2Na2CO3+O2,由方程式可知n(Na2O2)=0.018mol,则质量应大于0.018mol×78g/mol=1.404g,
如n(O2)=
| 0.224L |
| 22.4L/mol |
所以m(CaCO3)=0.02mol×100g/mol=2g,
则该同学测出的石灰石的纯度(CaCO3的质量分数)为
| 2g |
| 3g |
测得的质量分数偏大,可能原因是在除HCl时,NaHCO3与HCl反应生成了少量的CO2,使CO2的总体积增多,从而使石灰石的测定纯度偏大,
故答案为:>1.404;66.67%;在除HCl时,NaHCO3与HCl反应生成了少量的CO2,使CO2的总体积增多,从而使石灰石的测定纯度偏大.
点评:本题考查物质的制备方案的设计以及物质的含量的测定,侧重于学生的分析能力、实验能力和计算能力的考查,为高频考点,注意把握实验设计的目的和原理,把握实验操作的方法,结合反应的化学方程式计算,难度中等.

练习册系列答案
相关题目
下列关于化学反应速率和反应限度的说法正确的是( )
| A、不同形状的大理石与相同浓度的稀盐酸反应产生气体的速率:块状>粉末状 | |||
| B、不同浓度的硫酸溶解大小相同、形状相同铁片的速率:18 mol/L>3 mol/L | |||
| C、不同温度时,12%的过氧化氢溶液分解产生氧气的速率:60℃>30℃ | |||
D、2 mol SO2与足量O2在密闭容器中发生反应2SO2+O2
|
下列该各组离子中,因氧化还原反应在溶液中不能大量共存的是( )
A、H+、Na+、S2-、S
| ||||
B、Fe2+、H+、Cl-、N
| ||||
C、Na+、S
| ||||
D、Ba2+、N
|
我国赢得2008年第29届夏季奥运会的举办权.为向世界展现一个新的形象,某校同学提出下列建议:①开发新能源,减少化石燃料的燃烧;②开发生产无汞电池;③分类回收垃圾;④提倡使用一次性发泡塑料餐具和塑料袋;⑤提倡使用手帕,减少餐巾纸的使用;⑥提倡不使用含磷洗衣粉.你认为可以采纳的是( )
| A、①②③④⑥ | B、②③④⑤⑥ |
| C、①②③⑤⑥ | D、全部 |
下列有关盐酸与氢氧化钠溶液混合发生反应的说法中,不正确的是( )
| A、该反应是放热反应 |
| B、该反应是离子反应 |
| C、该反应属于复分解反应 |
| D、该反应属于氧化还原反应 |
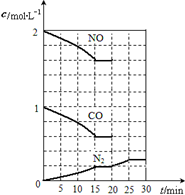 在铂-铑“三效”催化剂作用下,以下反应可以将汽车尾气中2种有
在铂-铑“三效”催化剂作用下,以下反应可以将汽车尾气中2种有