题目内容
书写离子方程式
(1)铜和足量浓硝酸反应的离子方程式为
(2)二氧化锰与足量浓盐酸反应的离子方程式为:
(3)向碳酸氢钾溶液中滴入少量澄清石灰水反应的离子方程式为:
(4)向明矾溶液中加入过量的氢氧化钡溶液反应的离子方程式为 .
(1)铜和足量浓硝酸反应的离子方程式为
(2)二氧化锰与足量浓盐酸反应的离子方程式为:
(3)向碳酸氢钾溶液中滴入少量澄清石灰水反应的离子方程式为:
(4)向明矾溶液中加入过量的氢氧化钡溶液反应的离子方程式为
考点:离子方程式的书写
专题:离子反应专题
分析:(1)铜和足量浓硝酸反应生成硝酸铜和二氧化氮和水;
(2)二氧化锰与足量浓盐酸反应生成氯气、氯化锰和水;
(3)向碳酸氢钾溶液中滴入少量澄清石灰水反应反应生成碳酸钙、碳酸钾和水;
(4)向明矾溶液中加入过量的氢氧化钡反应生成硫酸钡、偏铝酸钠和水.
(2)二氧化锰与足量浓盐酸反应生成氯气、氯化锰和水;
(3)向碳酸氢钾溶液中滴入少量澄清石灰水反应反应生成碳酸钙、碳酸钾和水;
(4)向明矾溶液中加入过量的氢氧化钡反应生成硫酸钡、偏铝酸钠和水.
解答:
解:(1)铜和足量浓硝酸反应的离子方程式为:Cu+4H++2NO3-═Cu2++2H2O+NO2↑;
故答案为:Cu+4H++2NO3-═Cu2++2H2O+NO2↑;
(2)二氧化锰与足量浓盐酸反应的离子方程式为:MnO2+4H++2Cl-=Mn2++Cl2↑+2H2O;
故答案为:MnO2+4H++2Cl-=Mn2++Cl2↑+2H2O;
(3)向碳酸氢钾溶液中滴入少量澄清石灰水反应的离子方程式为:2HCO3-+Ca2++2OH-=CO32-+2H2O+CaCO3↓;
故答案为:2HCO3-+Ca2++2OH-=CO32-+2H2O+CaCO3↓;
(4)向明矾溶液中加入过量的氢氧化钡溶液反应的离子方程式为:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O;
故答案为:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O.
故答案为:Cu+4H++2NO3-═Cu2++2H2O+NO2↑;
(2)二氧化锰与足量浓盐酸反应的离子方程式为:MnO2+4H++2Cl-=Mn2++Cl2↑+2H2O;
故答案为:MnO2+4H++2Cl-=Mn2++Cl2↑+2H2O;
(3)向碳酸氢钾溶液中滴入少量澄清石灰水反应的离子方程式为:2HCO3-+Ca2++2OH-=CO32-+2H2O+CaCO3↓;
故答案为:2HCO3-+Ca2++2OH-=CO32-+2H2O+CaCO3↓;
(4)向明矾溶液中加入过量的氢氧化钡溶液反应的离子方程式为:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O;
故答案为:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O.
点评:本题考查了离子方程式的书写,明确反应的实质是解题关键,注意D选项反应物的用量对反应的影响.

练习册系列答案
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
以NA代表阿伏加德罗常数,则关于热化学方程式 C2H2(g)+
O2(g)→2CO2(g)+H2O(l)△H=-1300kJ/mol的说法中,正确的是( )
| 5 |
| 2 |
| A、当10NA个电子转移时,该反应放出1300kJ的能量 |
| B、当1NA个水分子生成且为液体时,吸收1300kJ的能量 |
| C、当2NA个碳氧共用电子对生成时,放出1300kJ的能量 |
| D、当6NA个碳氧共用电子对生成时,放出1300kJ的能量 |
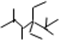 表示的分子名称是
表示的分子名称是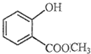 中含有的含氧官能团的名称为
中含有的含氧官能团的名称为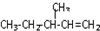 一定条件发生加聚反应时的化学方程式
一定条件发生加聚反应时的化学方程式
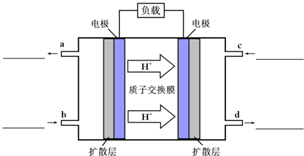 甲醇-空气燃料电池(DMFC)是一种高效能、轻污染电动汽车的车载电池,该燃料电池的电池反应式为:CH3OH(l)+
甲醇-空气燃料电池(DMFC)是一种高效能、轻污染电动汽车的车载电池,该燃料电池的电池反应式为:CH3OH(l)+