题目内容
下列物质中氧原子数目与93g Na2O中氧原子数一定相等的是( )
| A、67.2L CO2 |
| B、33g CO2 |
| C、80g SO3 |
| D、98g H2SO4 |
考点:物质的量的相关计算
专题:计算题
分析:n(Na2O)=
=1.5mol,根据N(O)=n(O)NA知,要使O原子个数相等,只要O原子的物质的量相等即可,根据O原子守恒得n(O)=n(Na2O)=1.5mol,只要给予的选项中O原子的物质的量为1.5mol即可.
| 93g |
| 62g/mol |
解答:
解:n(Na2O)=
=1.5mol,根据N(O)=n(O)NA知,要使O原子个数相等,只要O原子的物质的量相等即可,根据O原子守恒得n(O)=n(Na2O)=1.5mol,只要给予的选项中O原子的物质的量为1.5mol即可,
A.温度和压强未知,气体摩尔体积未知,所以无法计算二氧化碳中n(O),故A错误;
B.n(O)=2n(CO2)=2×
=1.5mol,故B正确;
C.n(O)=3n(SO3)=3×
=3mol,故C错误;
D.n(O)=4n(H2SO4)=4×
=4mol,故D错误;
故选B.
| 93g |
| 62g/mol |
A.温度和压强未知,气体摩尔体积未知,所以无法计算二氧化碳中n(O),故A错误;
B.n(O)=2n(CO2)=2×
| 33g |
| 44g/mol |
C.n(O)=3n(SO3)=3×
| 80g |
| 80g/mol |
D.n(O)=4n(H2SO4)=4×
| 98g |
| 98g/mol |
故选B.
点评:本题考查了物质的有关计算,灵活运用物质的量的有关公式即可解答,易错选项是A,有关气体体积的计算中要注意气体摩尔体积的适用范围及适用条件,为易错点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
25℃的下列溶液中,碱性最强的是( )
| A、100mLpH=11的Na2CO3溶液 |
| B、500mL c(OH-)=0.01mol/L的氨水溶液 |
| C、50mL 0.01mol/L Ba(OH)2溶液 |
| D、1L c(H+)=1×10-10mol/L的NaOH溶液 |
下列现象因发生加成反应而产生的是( )
| A、乙烯使酸性KMnO4溶液褪色 |
| B、乙烯使溴的四氯化碳溶液褪色 |
| C、将苯加入溴水中,振荡后水层接近无色 |
| D、甲烷与氯气混合,光照一段时间后黄绿色消失 |
某些建筑材料含有放射性元素氡(
Rn),会对人体产生一定危害.研究表明氡的α射线会致癌,WHO认定的19种致癌因素中,氡为其中之一,仅次于吸烟.该原子中中子数和质子数之差是( )
222 86 |
| A、136 | B、50 |
| C、86 | D、222 |
利用排空气法在烧瓶中收集了一定量的氨气,测得烧瓶中气体对氢气的相对密度是10.将此装有氨气的烧瓶倒立于水槽中,由于氨气溶于水造成烧瓶中液面上升,最后烧瓶中的水占据的空间是烧瓶体积的( )
A、
| ||
B、
| ||
C、
| ||
| D、全部 |
下列关于反应速率的说法中,错误的是( )
| A、反应速率可用于衡量化学反应的快慢 |
| B、决定反应速率的主要因素是温度和压强 |
| C、可逆反应达到化学平衡时,正、逆反应速率相等且不为零 |
| D、增大反应物浓度,提高反应物温度都能增大反应速率 |
将下列物质的水溶液蒸干并灼烧,不能得到该物质的是( )
| A、BaCl2 |
| B、NaHCO3 |
| C、Al(NO3)3 |
| D、Na2SO4 |
如图所示,△H1=-393.5kJ?mol-1,△H2=-395.4kJ?mol-1,下列说法正确的是( )


| A、石墨和金刚石互为同分异构体,相互之间的转化是化学变化 |
| B、C(s、石墨)═C(s、金刚石)△H=-1.9 kJ?mol-1 |
| C、金刚石硬度大于石墨,但金刚石的稳定性弱于石墨 |
| D、1 mol石墨的总键能比1 mol金刚石的总键能小1.9 kJ |
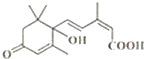 北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开,S-诱抗素的分子结构如图,下列关于该分子说法正确的是( )
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开,S-诱抗素的分子结构如图,下列关于该分子说法正确的是( )| A、分子式为C15H22O4 |
| B、1mol该物质最多可以消耗H2和Br2的量分别为4mol和3mol |
| C、含有碳碳双键、羟基、羰基、羧基 |
| D、该物质可以发生分子内酯化反应形成六元环,也可以发生缩聚反应和加聚反应 |