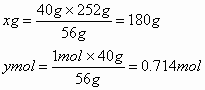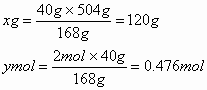题目内容
| |||||||||||
答案:
解析:
解析:
(1) |
由于反应Fe+2Fe3+===3Fe2+存在的可能性,题中“两者恰好完全反应”隐含三种情况, 设HNO3为xg,被还原的HNO3为y mo : Fe恰好与HNO3反应生成Fe(NO3)3 Fe+4HNO3===Fe(NO3)3+ NO↑+2H2O 56g 252g 1mol 40g xg ymol
硝酸质量分数为: 被还原的硝酸:0.714mol |
(2) |
Fe恰好与HNO3反应生成Fe(NO3)2 3Fe+8HNO3===3Fe(NO3)2+2NO↑+4H2O 168g 504g 2mol 40g xg ymol
硝酸质量分数为: 被还原的硝酸:0.476mol (2分) (3)Fe与HNO3完全反应生成Fe(NO3)2和Fe(NO3)3 硝酸质量分数介于20%~30%之间,被还原的硝酸介于:0.476mol~0.714mol之间.(2分) |

练习册系列答案
相关题目