题目内容
5.在相同条件下,下列排序不正确的是( )| A. | 酸性:H3PO4>H3AsO4 | |
| B. | 氧化性:HClO4>HClO | |
| C. | 还原性:Na2S>Na2SO3 | |
| D. | 结合H+能力:OH->CO${\;}_{3}^{2-}$>HCO${\;}_{3}^{-}$ |
分析 A.非金属性越强,最高价氧化物对应水合物的酸性越强;
B.高氯酸的氧化性较弱,次氯酸具有较强氧化性;
C.酸性条件下Na2SO3与Na2S溶液反应生成S单质,说明Na2S的还原性较强;
D.溶液碱性越强,越容易结合氢离子.
解答 解:A.非金属性P>As,则最高价氧化物对应水合物的酸性:H3PO4>H3AsO4,故A正确;
B.HClO具有强氧化性,HClO4的酸性较强,但是氧化性较弱,所以氧化性:HClO4<HClO,故B错误;
C.酸性条件下,Na2SO3与Na2S溶液反应生成S单质,反应中硫化钠被氧化,表现了还原性,则还原性:Na2S>Na2SO3,故C正确;
D.浓度相同时溶液碱性:OH->CO32->HCO3-,碱性越强,结合氢离子浓度越强,则结合H+能力:OH->CO32->HCO3-,故D正确;
故选B.
点评 本题考查了原子结构与元素周期律的应用,题目难度不大,明确元素周期律内容为解答关键,D为易错点,注意根据溶液碱性强弱分析,试题有利于培养学生的灵活应用能力.

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目
15.NaCl是重要的化工原料,可以制备一系列物质.有关下列流程的说法中,正确的是( )

| A. | NaHCO3的热稳定性好 | |
| B. | 如图所示转化涉及的反应都是氧化还原反应 | |
| C. | 常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应 | |
| D. | 石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂 |
16.将20mL2.5mol/LNaOH溶液加水稀释到100mL,稀释后的溶液中NaOH的物质的量浓度为( )
| A. | 1.0mol/L | B. | 0.5mol/L | C. | 0.2mol/L | D. | 0.1mol/L |
20.下列有关电解质溶液的说法中错误的是( )
| A. | 0.1mol•L-1的HCl溶液的pH=1 | |
| B. | 0.1mol•L-1的CH3COOH溶液中c(H+)<0.1mol•L-1 | |
| C. | 0.1mol•L-1的CH3COOH溶液和0.1mol•L-1的NaOH溶液等体积混合后溶液的pH=7 | |
| D. | 100mL0.1mol•L-1的H2SO4溶液中慢慢滴入100mL0.1mol•L-1的Ba(OH)溶液后,混合溶液的导电性几乎为零 |
2.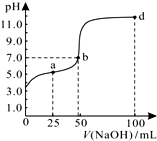 常温下,向100mL 0.01mol/L HA溶液中逐滴加入0.02mol/L NaOH溶液,混合溶液的pH变化情况如右图所示.下列判断正确的是( )
常温下,向100mL 0.01mol/L HA溶液中逐滴加入0.02mol/L NaOH溶液,混合溶液的pH变化情况如右图所示.下列判断正确的是( )
 常温下,向100mL 0.01mol/L HA溶液中逐滴加入0.02mol/L NaOH溶液,混合溶液的pH变化情况如右图所示.下列判断正确的是( )
常温下,向100mL 0.01mol/L HA溶液中逐滴加入0.02mol/L NaOH溶液,混合溶液的pH变化情况如右图所示.下列判断正确的是( )| A. | 由图中信息可知,HA可能为强酸 | |
| B. | a点对应的溶液中:2c(Na+)=c(A-)+c(HA) | |
| C. | b点对应的溶液中:c(Na+)=c(A-)+c(HA) | |
| D. | d点所对应的溶液中离子浓度的大小关系为:c(Na+)>c(A-)>c(OH-)>c(H+) |
9.室温下,用相同浓度的NaOH溶液,分别滴定100mL浓度均为0.1mol•L-1的三种酸(HM、HN和HR)溶液,滴定的曲线如图所示,下列判断错误的是( )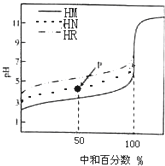

| A. | 三种酸的电离常数关系:KHM>KHN>KHR | |
| B. | pH=7时,三种溶液中:c(M-)>c(N-)>c(R-) | |
| C. | 滴定至P点时,溶液中:c(Na+)>c(N-)>c(HN)>c(H+)>c(OH-) | |
| D. | 当中和百分数达100%时,将三种溶液混合后:c(HM)+c(HN)+c(HR)=c(OH-)-c(H+) |
6.符合分子式C4H9Cl的同分异构体的数目为( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
7.现有三种有机物甲、乙、丙,其结构如图所示:

下列有关说法中正确的是( )

下列有关说法中正确的是( )
| A. | 均能与碳酸氢钠反应 | |
| B. | 只用碳酸钠溶液和银氨溶液能检验甲、乙、丙 | |
| C. | 与足量氢气反应,相同物质的量的甲、乙、丙消耗氢气的物质的量之比为3:4:3 | |
| D. | 甲的化学式为C11H13O2,乙含有两种含氧官能团 |