题目内容
9. 燃煤技术的改进,有助于合理控制温室效应、环境污染,并能进行资源化利用,还可重新获得燃料或重要工业产品.工业上以煤和水为原料通过一系列转化变为清洁能源氢气和工业原料甲醇.
燃煤技术的改进,有助于合理控制温室效应、环境污染,并能进行资源化利用,还可重新获得燃料或重要工业产品.工业上以煤和水为原料通过一系列转化变为清洁能源氢气和工业原料甲醇.(1)若碳的燃烧热为393.5KJ•mol-1,氢气的燃烧热为285.8KJ•mol-1.已知反应
C(s)+2H2O(g)$\frac{\underline{\;高温\;}}{\;}$ CO2(g)+2H2(g)△H>0,能否求出该反应的△H不能(填“能”或“不能”).若能则求出其△H(若不能请说明理由):上述反应与氢气燃烧热的反应中水的状态不同或H2O(g)?H2O(l)△H未知.
(2)工业上也可以仅利用上述反应得到的CO2和H2进一步合成甲醇,反应方程式为:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0
①工业生产过程中CO2和H2的转化率后者大(填“前者大”、“后者大”、“一样大”或“无法判断”),为了提高甲醇的产率可以采取的措施是降低温度、增大压强或分离产物(填两点).
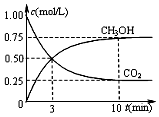
②在一恒温恒容密闭容器中充入1mol CO2和3mol H2进行上述反应.测得CO2和CH3OH(g)浓度随时间变化如图所示.
i.用H2表示0-3min内该反应的平均反应速率0.5mol•L-1•min-1.
ii.该温度下的平衡常数为5.33mol-2•L-2.10min后,保持温度不变,向该密闭容器中再充入1mol CO2(g)和1mol H2O(g),此时V正>V逆(填“>”、“<”或“=”).
iii.对于基元反应aA+bB?cC+dD而言,其某一时刻的瞬时速率计算公式如下:正反应速率为v正=k正•c(A)a•c(B)b;逆反应速率为v逆=k逆•c(C)c•c(D)d,其中k正、k逆为速率常数.若将上述反应视为基元反应则在上述条件下k逆:k正=3:16.反应进行到第3min时V正:V逆=36.
分析 (1)反应热与物质的聚集状态有关,聚集状态不同,反应热不同;
(2)①可逆反应中增大一种反应物浓度可以提高另一种反应物转化率,依据CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H<0为气体体积减小的、放热反应特点结合影响化学平衡移动的因素解答;
②ⅰ.图象中计算0-3min内甲醇的反应速率v(CH3OH)=$\frac{0.50mol/L}{3min}$,用H2表示0-3min内该反应的平均反应速率v(H2)=3v(CH3OH)=;
ⅱ.计算平衡时氢气、水的浓度,再根据K=$\frac{c(C{H}_{3}OH)c({H}_{2}O)}{c(C{O}_{2}){c}^{3}({H}_{2})}$计算平衡常数;
保持温度不变,向该密闭容器中再充入1mol CO2(g)和1mol H2O(g),相当于增大压强,增压平衡向气体系数小的方向移动;
iii.平衡时满足V正=V逆,v正=k正•c(A)a•c(B)b;V逆=k逆•c(C)c•c(D)d,则k逆:k正=$\frac{c(C{H}_{3}OH)c({H}_{2}O)}{c(C{O}_{2}){c}^{3}({H}_{2})}$=K;
计算3mim时各物质浓度,据此计算正逆反应瞬时速率之比.
解答 解:(1)反应热与物质的聚集状态有关,聚集状态不同,反应热不同,上述反应与氢气燃烧热的反应中水的状态不同,所以不能求出上述反应的焓变;
故答案为:不能;上述反应与氢气燃烧热的反应中水的状态不同或H2O(g)?H2O(l)△H未知;
(2)①C(s)+2H2O(g)?CO2(g)+2H2(g)△H>0生成二氧化碳和氢气的物质的量之比为1:2,而CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H<0,二氧化碳和氢气物质的量之比为1:3,相对与增大二氧化碳浓度,所以氢气的转化率大于二氧化碳转化率;
CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H<0为气体体积减小的、放热反应,要想提高甲醇的产率可以采取的措施是降低温度、增大压强使平衡向正向移动,分离产物平衡正向进行,提高甲醇的产率,
故答案为:后者大;降低温度;增大压强或分离产物;
②i.图象中计算0-3min内甲醇的反应速率v(CH3OH)=$\frac{0.50mol/L}{3min}$,用H2表示0-3min内该反应的平均反应速率v(H2)=3v(CH3OH)=0.5mol•L-1•min-1,
故答案为:0.5mol•L-1•min-1;
ⅱ.平衡时甲醇为0.75mol/L、二氧化碳为0.25mol/L,则:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
起始浓度(mol/L):1 3 0 0
变化浓度(mol/L):0.75 2.25 0.75 0.75
平衡浓度(mol/L):0.50 0.75 0.75 0.75
则平衡常数K=$\frac{c(C{H}_{3}OH)c({H}_{2}O)}{c(C{O}_{2}){c}^{3}({H}_{2})}$=$\frac{0.75×0.75}{0.25×0.7{5}^{3}}$=$\frac{16}{3}$=5.33;
保持温度不变,向该密闭容器中再充入1mol CO2(g)和1mol H2O(g),相当于增大压强,增压平衡向气体系数小的方向移动,即向正方向移动,此时V正>V逆,
故答案为:5.33;>;
iii.平衡时满足V正=V逆,v正=k正•c(A)a•c(B)b;V逆=k逆•c(C)c•c(D)d,
则k逆:k正=$\frac{{c}^{a}(A){c}^{b}(B)}{{c}^{c}(C){c}^{d}(D)}$=$\frac{1}{K}$=3:16;
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)
起始浓度(mol/L):1 3 0 0
变化浓度(mol/L):0.50 1.50 0.50 0.50
3min浓度(mol/L):0.50 1.50 0.50 0.50
v正=k正•c(A)a•c(B)b;
V逆=k逆•c(C)c•c(D)d;
V正:V逆=$\frac{{c}^{a}(A){c}^{b}(B)}{{c}^{c}(C){c}^{d}(D)}$×$\frac{{K}_{正}}{{K}_{逆}}$=$\frac{{K}_{正}}{{K}_{逆}}$×$\frac{0.5×1.{5}^{3}}{0.5×0.5}$=36;
故答案为:3:16; 36.
点评 本题为综合题,涉及反应热的计算、化学平衡平衡移动影响因素、化学平衡常数计算,题目难度中等,解题关键需掌握化学平衡理论,注意三段式的应用.

 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
下列说法不正确的是( )
| A. | CCl4起到萃取、富集I2的作用 | |
| B. | a中下层变无色,说明I2 转化为I- | |
| C. | Ⅲ中发生反应的离子方程式为:Br2+2I-═I2+2Br- | |
| D. | 只依据a、b中现象,不可以证明Cl2的氧化性比 Br2强 |
| A. | 向硫酸铜溶液中加入过量的NaHS溶液:Cu2++2HS-═CuS↓+H2S↑ | |
| B. | 向NH4Al(SO4)2溶液加入含两倍物质的量的Ba(OH)2溶液:Al3++2SO${\;}_{4}^{2-}$+4OH-+2Ba2+═2BaSO4↓+AlO${\;}_{2}^{-}$+2H2O | |
| C. | 向Na2S2O3溶液中通入足量的Cl2:S2O${\;}_{3}^{2-}$+2Cl2+3H2O═2SO${\;}_{3}^{2-}$+4Cl-+6H+ | |
| D. | 用石墨电极电解MgCl2溶液阴极电极反应:2H2O+2e-═H2↑+2OH- |
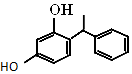 杨树生长迅速,高大挺拔,树冠有昂扬之势.其体内有一种有机物,结构如图所示.下列说法错误的是( )
杨树生长迅速,高大挺拔,树冠有昂扬之势.其体内有一种有机物,结构如图所示.下列说法错误的是( )| A. | 该有机物属于烃的衍生物 | |
| B. | 分子式为C14H14O2 | |
| C. | 1 mol该物质与溴水反应时最多能消耗2 mol的Br2 | |
| D. | 该有机物能与Na2CO3溶液反应,且生成的气体能使澄清石灰水变浑浊 |
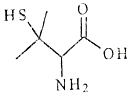
| A. | X的分子式为C5H10NO2S | |
| B. | X有2个手性碳原子 | |
| C. | X能发生加聚反应生成高分子化合物 | |
| D. | X既能与强酸反应,又能与强碱反应 |
| A. | Y4X10分子中,极性键和非极性键的个数比为10:4 | |
| B. | Z和W形成的多种化合物中只有一种能与水反应 | |
| C. | 25℃时,Z、W、X按原子个数比2:3:4形成的化合物的水溶液的pH=7 | |
| D. | 25℃时,等浓度的Z和Q的最高价氧化物对应水化物的水溶液中,水电离的c(H+)相等 |

 下图是部分短周期元素化合价与原子序数的关系图,请回答下列问题:
下图是部分短周期元素化合价与原子序数的关系图,请回答下列问题: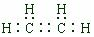 .
. ,A是一种常用的还原剂.向装有少量AgBr的试管中加入A的溶液,可观察到固体逐渐变黑,并有气泡产生,写出该反应的化学方程式4AgBr+N2H4=4Ag+N2↑+4HBr.b与c按原子数2和4构成分子B,已知A和B反应时生成无毒害物质,则该反应中氧化剂与还原剂的物质的量之比为1:2.
,A是一种常用的还原剂.向装有少量AgBr的试管中加入A的溶液,可观察到固体逐渐变黑,并有气泡产生,写出该反应的化学方程式4AgBr+N2H4=4Ag+N2↑+4HBr.b与c按原子数2和4构成分子B,已知A和B反应时生成无毒害物质,则该反应中氧化剂与还原剂的物质的量之比为1:2.