题目内容
4.赤铜矿的成分是Cu2O,辉铜矿的成分是Cu2S,将赤铜矿与辉铜矿混合加热有以下反应:Cu2S+2Cu2O$\frac{\underline{\;\;△\;\;}}{\;}$6Cu+SO2↑.对于该反应的下列说法正确的是( )| A. | 该反应中的氧化剂只有Cu2O | |
| B. | Cu2S在反应中既是氧化剂又是还原剂 | |
| C. | Cu既是氧化产物又是还原产物 | |
| D. | 生成1 mol Cu,转移2 mol电子 |
分析 Cu2S+2Cu2O$\frac{\underline{\;\;△\;\;}}{\;}$6Cu+SO2↑中,Cu元素的化合价降低,S元素的化合价升高,以此来解答.
解答 解:A.Cu元素的化合价降低,则Cu2O、Cu2S均为氧化剂,故A错误;
B.Cu2S+2Cu2O$\frac{\underline{\;\;△\;\;}}{\;}$6Cu+SO2↑中,Cu元素的化合价降低,S元素的化合价升高,则Cu2S在反应中既是氧化剂,又是还原剂,故B正确;
C.Cu元素得到电子被还原,则Cu为还原产物,故C错误;
D.Cu元素的化合价由+1降低到0价,所以生成1 mol Cu,转移1 mol电子,故D错误;
故选B.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重基本概念的考查,题目难度不大.

练习册系列答案
相关题目
13.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 64gCaC2中含有的共用电子对数为3NA | |
| B. | 标准状况下,11.2L己烷中含有的碳碳键数为2.5NA | |
| C. | 4.6gNO2在标准状况下,含有的分子数为0.1NA | |
| D. | 50mL12 mol•L-1盐酸与足量MnO2共热,转移的电子数为0.3NA |
14.某太阳能电池的工作原理如图所示.则光照时,失去电子的粒子是( )
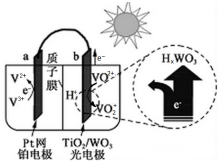

| A. | V2+ | B. | V3+ | C. | VO2+ | D. | VO2+ |
12.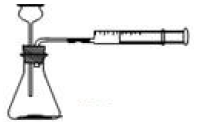 甲同学用0.1×10×25mm、质量分数≥99.5%的铝片和盐酸用下图装置反应制取H2,实验现象如表:
甲同学用0.1×10×25mm、质量分数≥99.5%的铝片和盐酸用下图装置反应制取H2,实验现象如表:
(1)写出上述铝与盐酸反应的离子方程式2Al+6H+=2Al3++3H2↑.
(2)实验开始1min内反应速率很慢,原因是温度低,铝片表面的三氧化二铝先和盐酸反应没有气体生成
(3)反应1~15min内,反应速率逐渐加快,原因是反应放热,温度升高.
(4)反应10min时注射器读数为448mL(假设为标准状况),则注射器中氢气的物质的量浓度为0.04mol/L.用氢气表示的化学反应速率为0.004mol/(L•min)(1/22.4=0.04)
(5)乙同学认为用铝粉代替铝片实验效率更高,原因是_铝粉与盐酸接触面积更大,反应速率加快
(6)丙同学认为甲、乙两位同学收集的氢气都不纯,含有杂质的化学式为HCl,H2O.
 甲同学用0.1×10×25mm、质量分数≥99.5%的铝片和盐酸用下图装置反应制取H2,实验现象如表:
甲同学用0.1×10×25mm、质量分数≥99.5%的铝片和盐酸用下图装置反应制取H2,实验现象如表: | 1min | 2min | 5min | 15min | 20min |
| 3mol•L-1HCl | 少量气泡 | 较多气泡 | 大量气泡 | 反应剧烈 | 铝片耗尽 |
(2)实验开始1min内反应速率很慢,原因是温度低,铝片表面的三氧化二铝先和盐酸反应没有气体生成
(3)反应1~15min内,反应速率逐渐加快,原因是反应放热,温度升高.
(4)反应10min时注射器读数为448mL(假设为标准状况),则注射器中氢气的物质的量浓度为0.04mol/L.用氢气表示的化学反应速率为0.004mol/(L•min)(1/22.4=0.04)
(5)乙同学认为用铝粉代替铝片实验效率更高,原因是_铝粉与盐酸接触面积更大,反应速率加快
(6)丙同学认为甲、乙两位同学收集的氢气都不纯,含有杂质的化学式为HCl,H2O.
19.已知25℃物质的溶度积常数为:FeS:Ksp=6.3×10-18;CuS:Ksp=1.3×10-36;ZnS:Ksp=1.6×10-24.下列说法正确的是( )
| A. | 相同温度下,CuS的溶解度小于ZnS的溶解度 | |
| B. | 除去工业废水中的Fe2+,可以选用CuS做沉淀剂 | |
| C. | 足量CuSO4溶解在0.1mol/L的H2S溶液中,Cu2+能达到的最大浓度为1.3×10-35mol/L | |
| D. | 在ZnS的饱和溶液中,加入FeCl2溶液,一定不产生FeS沉淀 |
9.已知反应:2Fe3++2I-?2Fe2++I2,用KI溶液和FeCl3溶液进行如下实验.下列说法中,不正确的是( )
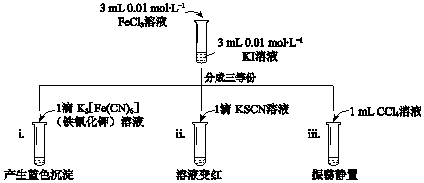

| A. | 实验i中现象说明有Fe2+生成 | |
| B. | 实验ii中现象说明反应后溶液中含有Fe3+ | |
| C. | 实验iii水溶液中c(Fe2+)大于i中c(Fe2+) | |
| D. | 实验iii中再加入4滴0.1 mol•L-1 FeCl2溶液,振荡静置,CCl4层溶液颜色无变化 |
13.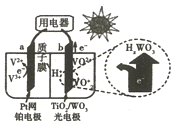 如图是用于航天飞行器中的一种全天候太阳能电化学电池在光照时的工作原理.下列说法正确的是( )
如图是用于航天飞行器中的一种全天候太阳能电化学电池在光照时的工作原理.下列说法正确的是( )
 如图是用于航天飞行器中的一种全天候太阳能电化学电池在光照时的工作原理.下列说法正确的是( )
如图是用于航天飞行器中的一种全天候太阳能电化学电池在光照时的工作原理.下列说法正确的是( )| A. | 该电池与硅太阳能电池供电原理相同 | |
| B. | 光照时,H+由a极室通过质子膜进入b极室 | |
| C. | 夜间无光照时,a电极流出电子 | |
| D. | 光照时,b极反应式是VO2++2OH--e-=VO2++H2O |
14.检验HCl气体中是否混有Cl2的正确方法为( )
| A. | 将气体通入AgNO3溶液 | B. | 将气体通过干燥的有色布条 | ||
| C. | 将气体通过干燥的红色石蕊试纸 | D. | 将气体通入含有KSCN的FeCl2溶液 |