��Ŀ����
��������ʱ�����£�N2H4��Ϊȼ�ϺͶ��������������������߷�Ӧ���ɵ�������̬ˮ����֪��
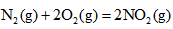 ��H=+67.7kJ��mol-1
��H=+67.7kJ��mol-1
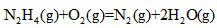 ��H=-543kJ��mol-1
��H=-543kJ��mol-1
 ��H=-269kJ��mol-1
��H=-269kJ��mol-1
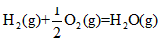 ��H=-242kJ��mol-1
��H=-242kJ��mol-1
��1���ºͷ�Ӧ���Ȼ�ѧ����ʽΪ��______________ ��
��2��������Ϊ���÷�������������������Ӧ�ͷŵ����������ºͷ�����Ӧ���Ȼ�ѧ����ʽΪ��______________ ��
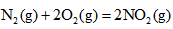 ��H=+67.7kJ��mol-1
��H=+67.7kJ��mol-1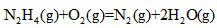 ��H=-543kJ��mol-1
��H=-543kJ��mol-1 ��H=-269kJ��mol-1
��H=-269kJ��mol-1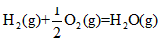 ��H=-242kJ��mol-1
��H=-242kJ��mol-1 ��1���ºͷ�Ӧ���Ȼ�ѧ����ʽΪ��______________ ��
��2��������Ϊ���÷�������������������Ӧ�ͷŵ����������ºͷ�����Ӧ���Ȼ�ѧ����ʽΪ��______________ ��
(1)2N2H4(g) + 2NO2(g) == 3N2(g) + 4H2O(g) ��H = -1153.7 kJ��mol-1
(2)N2H4(g) + 2F2(g) == N2(g) + 4HF(g) ��H = -1135 kJ��mol-1
(2)N2H4(g) + 2F2(g) == N2(g) + 4HF(g) ��H = -1135 kJ��mol-1

��ϰ��ϵ�д�
�����Ŀ


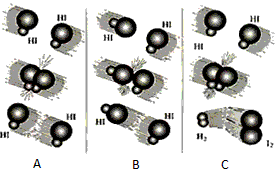
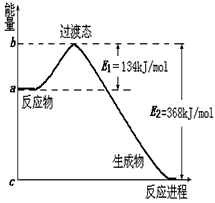
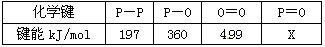
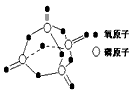

 H = -142��9 kJ��mol-1
H = -142��9 kJ��mol-1 H = +285��8 kJ��mol-1
H = +285��8 kJ��mol-1