题目内容
把足量的铁粉投入到稀盐酸和氯化铜的混合溶液中,充分反应后,残余固体的质量与原来加入 的铁粉质量相等,则原溶液中H+ 和Cl-的物质的量之比为( )
A.1∶4 B.1∶7 C.1∶8 D.2∶5
C
【解析】
试题分析:在盐酸和氯化铜的混合溶液中加入足量的铁粉,分别发生:2H++Fe=Fe2++H2↑,Fe+Cu2+=Fe2++Cu,其充分反应,所得滤渣的质量与原铁粉的质量恰好相等,则消耗的铁的质量应等于生成的铜的质量,令Cu的质量为64g,其物质的量为1mol,则
Fe + Cu2+ = Fe2+ + Cu
56g 1mol 64g 故溶液中n(Cu2+)=1mol
所以与酸反应的Fe的质量为64g-56g=8g,其物质的量为8g÷56g/mol=1/7mol,由2H++Fe=Fe2++H2↑,可知n(H+)=2/7mol,根据电荷守恒可得n(Cl-)=n(H+)+2n(Cu2+)=2/7mol+2mol=16/7mol,故原混合溶液中c(H+):c(Cl-)=2/7mol:16/7mol=1:8,故C项正确。
考点:本题考查混合物的计算、根据化学方程式的计算。

(18分)某校化学实验兴趣小组在“探究卤索单质的氧化性”的系列实验中发现:在足量的稀氯化亚铁溶液中,加入l~2滴溴水,振荡后溶液呈黄色。
提出问题 Fe3+、Br2谁的氧化性更强?
(1 )猜 想: ①甲同学认为氧化性:Fe3+>Br2,故上述实验现象不是发生化学反应所致,则溶液呈黄色是含 (填化学式,下同)所致。
②乙同学认为氧化性:Br2>Fe3+,故上述实验现象是发生化学反应所致,则溶液呈黄色是含 所致。
(2)设计实验并验证
丙同学为验证乙同学的观点,选用下列某些试剂设计出两种方案进行实验,并通过观察实验现象,证明了乙同学的观点确实是正确的。
供选用的试剂:a.酚酞试液;b.CCl4;c.无水酒精;d.KSCN溶液。
请你在下表中写出丙同学选用的试剂及实验中观察到的现象。(试剂填序号)
| 选用试剂 | 实验现象 |
方案1 |
|
|
方案2 |
|
|
(3)结论:氧化性:Br2>Fe3+。故在足量的稀氯化亚铁溶液中,加入l~2滴溴水,溶液呈黄色所发生的离子反应方程式为 。
(4)实验后的思考
①根据上述实验推测,若在溴化亚铁溶液中通入氯气,首先被氧化的离子是:
(填离子的化学式)。
②在100 mL FeBr2溶液中通入2.24 L Cl2(标准状况),溶液中有1/2的Br-被氧气成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为 。
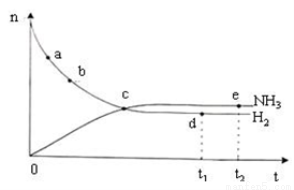
 2NH3(g) △H<0, n(NH3)和n(H2)随时间变化的关系曲线图。点d(t1时刻)和点e(t2时刻)处n(N2)不一样
2NH3(g) △H<0, n(NH3)和n(H2)随时间变化的关系曲线图。点d(t1时刻)和点e(t2时刻)处n(N2)不一样 Fe(SCN)3具有反应迅速、现象明显等特点,是检验Fe3+常用的方法之一。某化学兴趣小组为探究Fe(SCN)3的性质,做了以下实验:
Fe(SCN)3具有反应迅速、现象明显等特点,是检验Fe3+常用的方法之一。某化学兴趣小组为探究Fe(SCN)3的性质,做了以下实验: