题目内容
一定质量的某烃完全燃烧需要24g氧气,生成9g水,则该烃的分子式为( )
| A、C2H6 |
| B、C3H8 |
| C、C4H6 |
| D、C5H10 |
考点:有关有机物分子式确定的计算
专题:烃及其衍生物的燃烧规律
分析:根据n=
计算出该烃完全燃烧消耗氧气、生成水的物质的量,设出该烃的物质的量为n、分子式为CxHy,然后根据烃的燃烧关系式、氢原子守恒列式计算出x、y的关系.
| m |
| M |
解答:
解:24g氧气的物质的量为:
=0.75mol,
9g水的物质的量为:
=0.5mol,
设该烃的分子式为CxHy,其物质的量为n,烃的燃烧通式为:CxHy~(x+
)O2,
则:①n×(x+
)=0.75mol,
根据氢原子守恒可得:②n×
=0.5mol,
根据
可得:
=
,
整理可得:y=2x,
即氢原子为碳原子数的2倍,该烃的通式为:CnH2n,满足条件的D,
故选D.
| 24g |
| 32g/mol |
9g水的物质的量为:
| 9g |
| 18g/mol |
设该烃的分子式为CxHy,其物质的量为n,烃的燃烧通式为:CxHy~(x+
| y |
| 4 |
则:①n×(x+
| y |
| 4 |
根据氢原子守恒可得:②n×
| y |
| 2 |
根据
| ① |
| ② |
n(x+
| ||
ny×
|
| 3 |
| 2 |
整理可得:y=2x,
即氢原子为碳原子数的2倍,该烃的通式为:CnH2n,满足条件的D,
故选D.
点评:本题考查了有机物燃烧的计算、有机物分子式的确定,题目难度中等,注意掌握常见有机物分子式的计算方法,明确烃的燃烧方程式的应用方法,试题有利于提高学生的分析、理解能力及化学计算能力.

练习册系列答案
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
下列基本的实验操作不正确的是( )
A、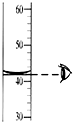 液体体积读数 |
B、 熄灭酒精灯 |
C、 检查气密性 |
D、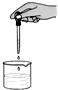 滴加液体 |
下列与化学反应能量变化相关的叙述正确的是( )
| A、由H+(aq)+OH-(aq)═H2O(l)△H═-57.3 kJ?mol-1,则向含0.1molHCl的盐酸中加入4.0gNaOH固体,放出热量等于5.73kJ |
| B、等量H2在O2中完全燃烧生成H2O(g)与生成H2O(l),放出的能量相同 |
| C、同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H不同 |
| D、氢气的燃烧热为285.8 kJ?mol-1,则水分解的热化学方程式为:2H2O(l)═2H2(g)+O2(g)△H═+571.6 kJ?mol-1 |
下列实验方案中,合理的是( )
| A、可用生石灰除去乙酸中少量水 |
| B、用5 mL苯与1mL浓溴水反应(Fe粉作催化剂)制溴苯 |
| C、向适量浓硝酸、浓硫酸的混合物中逐滴加人苯,在50-60℃的水浴中加热以制取硝基苯 |
| D、无水乙醇与6mol/L硫酸按体积比1:3混合迅速加热到170℃制取乙烯 |
将pH=4的盐酸X L分别与下列三种溶液混合后,混合液均呈中性:①1×10-4 mol/L的氨水Y L ②c(OH-)=1×10-4mol/L的氨水Z L ③c(OH-)=1×10-4 mol/L的Ba(OH)2溶液W L.其中X、Y、Z、W的关系正确的是( )
| A、Y>X=W>Z |
| B、X=Y>Z>W |
| C、X=Y>W>Z |
| D、Z>X=W>Y |
亚硒酸钠(Na2SeO3)能消除加速人体衰老的活性氧,亚硒酸钠中硒元素(Se)的化合价为( )
| A、+2 | B、+3 | C、+4 | D、+5 |
下列变化过程中,只破坏共价键的是( )
| A、干冰升华 |
| B、NaCl颗粒被粉碎 |
| C、HCl溶于水 |
| D、NH4HCO3久置逐渐减少 |
下列各烃分别与H2完全加成,不能生成2,2,3-三甲基戊烷的是( )
A、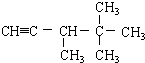 |
B、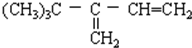 |
| C、CH2=CHC(CH3)2CH(CH3)2 |
D、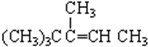 |